 CARBOIDRATOS
CARBOIDRATOS
São compostos de função mista poliálcool-aldeído
ou poliálcool-cetona, assim como todos os compostos que, por hidrólise,
produzem os referidos compostos de função mista.
Os carboidratos são assim chamados porque
freqüentemente apresentam fórmula mínima CH2O, que sugere um
hidrato de carbono.
1.
Classificação
–
Oses: Monossacarídeos
–
Osídeos

I.
Oses
Açúcares que não se hidrolisam.
Ex.: glicose, frutose, galactose.
●
Aldoses:
apresentam o grupo aldeído. De acordo com o número de átomos de carbono,
classificam-se em aldotriose (3C); aldotetrose (4C); aldohexose (6C)...
●
Cetoses:
apresentam o grupo cetônico, classificam-se também em cetotriose (3C);
cetohexose (6C)...
Costuma-se representar as fórmulas das aldoses e
cetoses na vertical. Nestas fórmulas, um círculo representa o grupo
aldeído, o sinal representa o grupo cetona e um traço, o grupo
hidroxila.
Assim, as fórmulas de
aldotriose e da cetotriose:
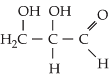
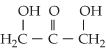
são representadas por:
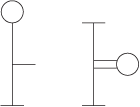
II. Osídeos
Açúcares que hidrolisam
produzindo oses. Classificam-se em:
●
Holosídeos:
osídeos que, por hidrólise, forne- cem somente oses.
Subdividem-se em:
Dissacarídeos
Açúcares que se hidrolisam,
fornecendo duas moléculas de monossacarídeos.
Exemplo
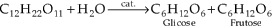
Polissacarídeos
Açúcares que se hidrolisam,
formando mais de duas moléculas de monossacarídios.
Exemplo

●
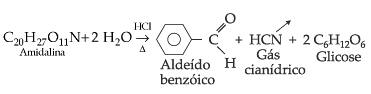
Heterosídeos:
Osídeos que, por hidrólise, fornecem outros compostos além das oses.
2. Isomeria nos Açúcares
Uma
aldose com n átomos de carbono apresenta (n – 2) átomos de carbono quirais
diferentes e, portanto, 2n – 2 isômeros opticamente ativos.
Uma
cetose com n átomos de carbono apresenta (n – 3) átomos de carbono quirais
diferentes e, portanto, 2n – 3 isômeros opticamente ativos.
Uma
cetohexose apresenta três átomos de carbono quirais diferentes. São
possíveis, portanto, oito isômeros. Destes oito isômeros, apenas a frutose é
abundante na natureza.
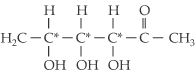
Uma
aldohexose apresenta quatro átomos de carbono quirais diferentes. São
possíveis, portanto, 16 isômeros. Na natureza são abundantes apenas três:
glicose, manose e galactose.
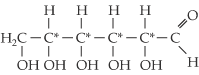
3. Estrutura dos Monossacarídeos
Por
convenção, o estudo das estruturas das oses é feito a partir da aldose mais
simples, que é o aldeído glicérico (aldotriose).
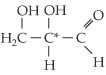
Como
vemos, o aldeído glicérico apresenta 1 átomo de C quiral e, como tal, pode
ser representado por dois antípodas ópticos: o dextrogiro (ald. d
glicérico) e o levogiro (ald. l glicérico).
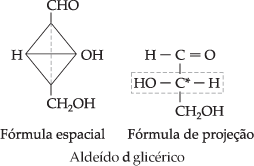
Inicialmente, representaremos as fórmulas de projeção dos antípodas dos
aldeídos glicéricos, na vertical:
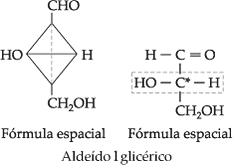
As oses
têm suas estruturas convencionadas a partir dos aldeídos glicéricos.
A
cadeia carbônica poderá ser aumentada a partir do grupo aldeídico.
Assim,
obteremos, a partir do aldeído d glicérico, uma aldotetrose em que a
base (os últimos carbonos) da cadeia será idêntica à da aldotriose inicial.
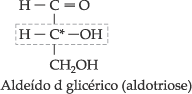
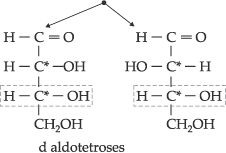
As duas
aldotetroses levarão a letra d em sua nomenclatura, pois são
provenientes do aldeído d glicérico.
Da
mesma forma, as aldotetroses, provenientes do ald. l glicérico,
levarão a letra l em sua nomenclatura oficial.
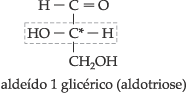
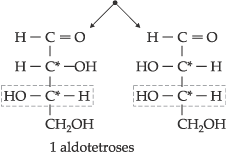
Seguindo o mesmo raciocínio, poderemos obter aldopentose a partir do
aldotetrose, ou ainda, aldohexose a partir de aldopentose, e assim
sucessivamente.
Portanto, uma ose levará a letra d e l em seu nome, de acordo
com a origem, isto é, se pertencer à série do aldeído d ou l
glicérico, respectivamente.
Reconhecemos pela estrutura a série a que pertence uma ose pela posição da
penúltima oxidrila: se estiver à direita da cadeia, conven- cionamos
pertencer à série d e levará tal letra em sua nomenclatura e, se
estiver à esquerda da cadeia, a ose levará a letra l e pertencerá,
portanto, à série l.
Outros exemplos
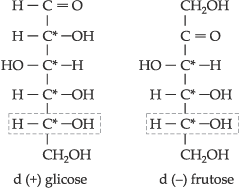
Pelas
representações anteriores, notamos que a glicose e a frutose pertencem à
série d das oses, porém a primeira é dextrogira (+) e a segunda é
levogira (–). Portanto, as letras d e l no nome das oses nada
têm a ver com a rotação do plano da luz polarizada.
4. Simplificação das Fórmulas Estruturais das Oses
Pode
ser feita representando-se a cadeia principal por uma linha vertical e as
hidroxilas por pequenos traços à direita ou à esquerda dessa vertical.
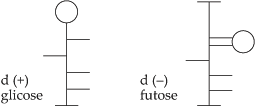
5.
Propriedades Físicas dos Glicídios
As oses
são compostos cristalinos, incolores, solúveis na água e pouco solúveis em
solventes orgânicos. Apresentam sabor adocicado. Os dissacarídeos apresentam
propriedades semelhantes.
Os
polissacarídeos são amorfos insolúveis em água sem sabor.
I. Oses Epímeras
São
oses que diferem somente na configuração de um único carbono quiral.
Exemplo
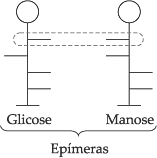
6. Estudo Geral dos Oses e Osídeos
I. Glicose
C6H12O6
 glucose
dextrogira, açúcar da uva.
glucose
dextrogira, açúcar da uva.
Ocorre
no mel e frutos doces; é obtida pela hidrólise do amido em meio ácido.
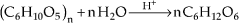
Sua
aplicação é na fabricação de álcool etílico, alimentação de crianças, de
atletas (após as competições).
II. Frutose
C6H12O6
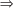 levulose
(ocorre no mel, nos frutos doces, sempre na forma d (–).
levulose
(ocorre no mel, nos frutos doces, sempre na forma d (–).
III. Sacarose
C12H22O11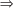 açúcar de cana, açúcar comum: ocorre em plantas, principalmente, a
cana-de-açúcar e a beterraba.
açúcar de cana, açúcar comum: ocorre em plantas, principalmente, a
cana-de-açúcar e a beterraba.
Sua
obtenção obedece à seqüência:
a)
obtenção da garapa;
b)
precipitação das proteínas e ácidos livres, por tratamento com hidróxido de
cálcio;
c)
eliminação do excesso de Ca(OH)2 borbulhando CO2
(precipita CaCO3);
d)
filtração e cristalização por centrifugação, separando-se o melaço do
açúcar.
Sua
aplicação é na alimentação e na fabricação de álcool etílico.
IV. Celulose
(C6H10O5)n
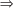 ocorre em
todos os vegetais. O algodão é praticamente celulose (95%).
ocorre em
todos os vegetais. O algodão é praticamente celulose (95%).
– A sua
massa molecular média é de 400.000. A celulose praticamente não é digerível
pelo organismo humano.
– Sua
aplicação é na fabricação do papel e no tecido de algodão.
– Usado
na preparação do algodão, pólvora (explosivo potente); na fabricação de
celulóides, filmes, sedas artificiais e na fabricação de vidros de segurança
para carros (dois vidros colados com acetato de celulose).
V. Amido
(C6H10O5)n
 ocorre nas
reservas dos vegetais; sua aplicação é na alimentação e na fabricação de
cola.
ocorre nas
reservas dos vegetais; sua aplicação é na alimentação e na fabricação de
cola.
Home | Proteínas | Lipídios | Carboidratos
Este site foi atualizado em
04/03/19