PROFESSOR
PAULO CESAR
|
PROFESSOR PAULO CESAR |
|
|
|
|
|
|
|
I.Dipolo-dipolo (ou Dipolo permanente - Dipolo permanente) | |
|
II.Dipolo-dipolo induzido (ou Dipolo induzido – Dipolo induzido) ou ainda Forças de dispersão ou Forças de London | |
|
III.Pontes de Hidrogênio ou Ligação de Hidrogênio |
Forças
Intermoleculares
I. Dipolo- Dipolo
As moléculas de alguns materiais, embora eletricamente neutras, podem possuir um dipolo elétrico permanente. Devido a alguma distorção na distribuição da carga elétrica, um lado da molécula e ligeiramente mais "positivo" e o outro é ligeiramente mais "negativo". A tendência é destas moléculas se alinharem, e interagirem umas com as outras, por atração eletrostática entre os dipolos opostos.
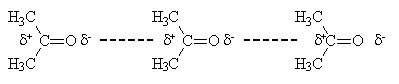
Em algumas moléculas o centro das cargas positivas não coincide com o centro das cargas negativas, mesmo na ausência de campos elétricos externos.
Estas moléculas são chamadas polares, e possuem momento de dipolo permanente.
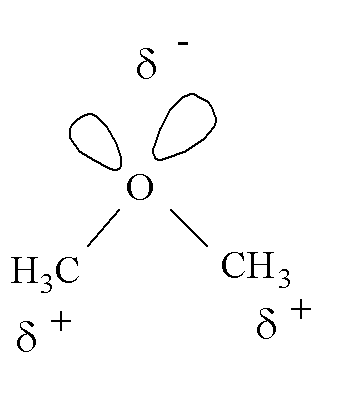
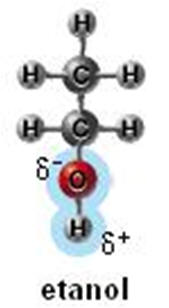
Note que o oxigênio é mais eletronegativo que o carbono. Isto torna a ligação C-O polar.
As moléculas do éter representado acima não podem realizar ligações de hidrogênio porque falta o H deficiente em elétrons (mas possuem o par eletrônico não ligante disponível para a formação da ligação de hidrogênio).
II. Dipolo – Dipolo Induzido
Ocorre quando a molécula é apolar.
A presença de moléculas que tem dipolos permanentes podem distorcer a distribuição de carga elétrica em outras moléculas vizinhas, mesmo as que não possuem dipolos (apolares), através de uma polarização induzida.
O momento de dipolo de um átomo ou molécula apolar num campo elétrico externo é chamado de Dipolo Induzido.
Se o campo elétrico for não uniforme, haverá uma força elétrica resultante não nula atuando sobre o dipolo: Esta é a força responsável pela conhecida atração de pequeninos pedaços de papel por um pente carregado

Normalmente hidrocarbonetos (substâncias formadas apenas por Hidrogênio e Carbono) são consideradas apolares: apesar de o átomo de carbono ser mais eletronegativo que o átomo de hidrogênio, esta diferença de eletronegatividade não é significativa.
Nesta situação (interação dipolo induzido-dipolo induzido) o que importa é a área superficial. Quanto maior for esta área, maior será a interação.
Em um determinado instante, o centro de carga negativa dos elétrons e de carga positiva do núcleo atômico poderia não coincidir. Esta flutuação eletrônica poderia transformar as moléculas apolares, tal como o benzeno, em dipolos tempo-dependentes, mesmo que, após um certo intervalo de tempo, a polarização média seja zero. Estes dipolos instantâneos não podem orientar-se para um alinhamento de suas moléculas, mas eles podem induzir a polarização das moléculas adjacentes, resultando em forças atrativas.
III. Ligações de Hidrogênio
Quando um átomo de hidrogênio liga-se por covalência a um átomo mais eletronegativo mantém uma afinidade residual por outro átomo eletronegativo, apresentando uma tendência à carga positiva. Por exemplo, um átomo de hidrogênio (receptor de elétrons) pode atuar como uma ponte entre dois átomos de oxigênio (doador de elétrons), ligando-se a um deles por ligação covalente e ao outro por forças eletrostáticas.
Ocorre quando existe um átomo de H deficiente em elétrons e um par eletrônico disponível (principalmente em grupos -OH e -NH ).
Ligação Hidrogênio
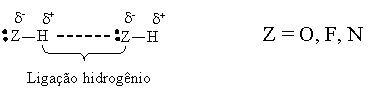
Ocorre entre átomos de hidrogênio ligados a elementos como o oxigênio, flúor ou nitrogênio, com átomos de O, N ou F de outras moléculas. Esta interação é a mais intensa de todas as forças intermoleculares
Água
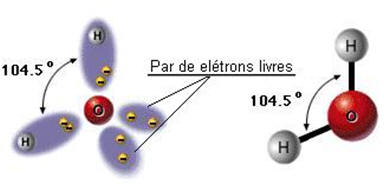
A água, deve possuir um tipo de interação diferenciado.
O que acontece é que os hidrogênios ligados ao oxigênio é que formam o lado "positivo" do dipolo permanente desta molécula. O átomo de hidrogênio é formado por apenas um próton e um elétron. Como o elétron é fortemente atraído pelo oxigênio, na água, este próton encontra-se desprotegido.
A água possui, então, um dipolo bastante forte, com uma das cargas (positiva) bastante localizada. Este próton pode interagir com as regiões negativas (o oxigênio) de outras moléculas de água, resultando em uma forte rede de ligações intermoleculares.
Como conseqüência das fortes interações intermoleculares, a água apresenta algumas propriedades especiais. Alguns insetos, por exemplo, podem andar sobre ela. Uma lâmina de barbear, se colocada horizontalmente, também flutua na água. Isto deve-se à tensão superficial da água.
Tensão Superficial da Água

Uma propriedade que faz com o líquido se comporte como se tivesse uma membrana elástica em sua superfície. Este fenômeno pode ser observado em quase todos os líquidos, e é o responsável pela forma esférica de gotas ou bolhas do líquido.
A razão é que as moléculas de água interagem muito mais fortemente com suas vizinhas do que com as moléculas do ar, na interface. As moléculas que estão no interior da gota, por exemplo, interagem com outras moléculas em todas as direções; as moléculas da superfície, por outro lado, interagem somente com moléculas que estão nas suas laterais ou logo abaixo.
Este “desbalanço” de forças intermoleculares faz com que estas moléculas, da superfície, sejam atraídas para o interior do líquido. Para se remover estas moléculas da superfície é necessário uma certa quantidade mínima de energia - a tensão superficial. Para a água, isto corresponde a 0,07275 joules/m2, a 20oC. Líquidos orgânicos, como o benzeno ou o tolueno, tem valores menores de tensão superficial, já que suas interações intermoleculares são mais fracas.
3. Ponto de Ebulição
Quanto mais fortes forem as ligações intermoleculares, mais elevada será a temperatura de ebulição.
Exemplo
|
Substância |
Fórmula |
Massa molar |
Temperatura de Ebulição (ºC) |
|
Propano |
CH3CH2CH3 |
44 |
- 45ºC |
|
Metoximetano |
CH3 – O – CH3 |
46 |
- 25ºC |
|
Etanal |
CH3CHO |
44 |
+ 20ºC |
|
Etanol |
CH3CH2OH |
46 |
+ 78ºC |
Quanto mais “esférica” for a molécula, menor será seu ponto de ebulição, já que as forças de Van der Waals são mais eficientes quanto maior for a superfície de contato.
A água tem comportamento excepcional quando comparado aos pontos de ebulição de substâncias moleculares semelhantes. Podemos notar que, caso a água mantivesse a linearidade do gráfico, sendo essa linearidade ditada pela massa molecular dos compostos da mesma família, teria um ponto de ebulição próximo de 100 C!. Caso isso fosse verdade, a Terra não teria lagos, rios ou oceanos, e a água existiria na Terra somente no estado gasoso, mesmo nos pólos do Norte e Sul
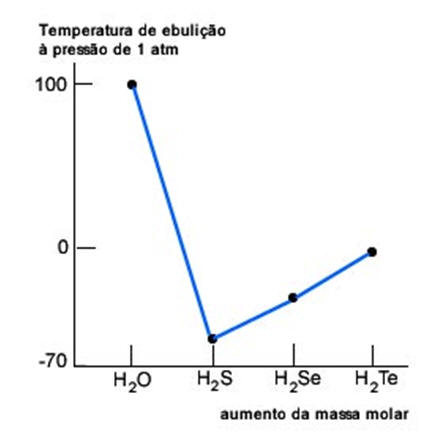
Ao contrário da água, o sulfeto de hidrogênio, bem como H2Se e o H2Te, são incapazes de formar ligações intermoleculares fortes. Ligações de hidrogênio, de forma apreciável, só são encontradas nas moléculas que contêm os elementos mais eletronegativos, como o flúor, o oxigênio e o nitrogênio. As propriedades das substancias com ligação H-X de polaridade elevada, semelhante à da água, como a amônia e o fluoreto de hidrogênio, são também influenciadas pelas ligações de hidrogênio, e muitas de suas propriedades, nos estados sólidos e líquidos, resultam das interações dipolo-dipolo entre suas moléculas.
Os Hidrocarbonetos possuem a seguinte relação dos seus Pontos de Ebulição(PE):
|
Proporcional ao tamanho da cadeia. MAIOR CADEIA = MAIOR P.E. (Área de contato maior, entre as moléculas!) | |
|
Para hidrocarbonetos ramificados: MAIOR NÚMERO DE RAMIFICAÇÕES = MENOR P.E. (Área de contato menor, entre as moléculas!) |
4. Ponto de Fusão
As substâncias iônicas tem P.F , P.E elevados e são geralmente sólidas porque os cátions e os ânions se atraem fortemente e a dificuldade de afastar os cátions e os ânions se traduz na dificuldade de fundir e de ferver as substâncias iônicas.
Pelo contrário , as substâncias orgânicas são em geral covalentes e freqüentemente apolares; em conseqüência tem P.F e P.E. baixos e são geralmente líquidos ou gases.
5. Solubilidade
A solubilidade é largamente afetada pela estrutura química dos compostos, sendo que o grau de solubilidade em água dos éteres glicólicos varia de acordo com o comprimento da cadeia do grupo alquila e o número de átomos de oxigênio presentes na molécula. Porém, isômeros podem apresentar diferenças.
"O semelhante dissolve o semelhante”

Mãos sujas de graxas (apolares) dever ser limpas com um solvente apolar como por exemplo a gasolina que é uma mistura de hidrocarbonetos.
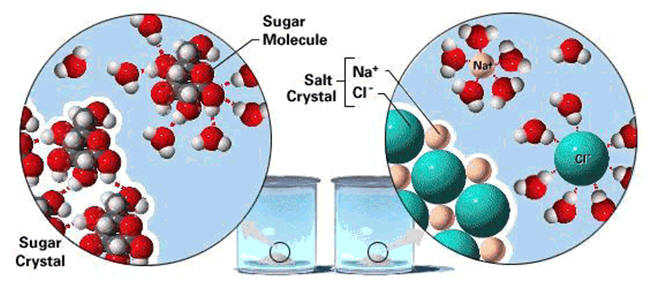
Substância polar dissolve substância polar e não dissolve ou dissolve pouca quantidade de substância apolar. Substância apolar dissolve substância apolar e não dissolve ou dissolve pouca quantidade de substância polar.
 Existem
Existem
Basicamente dois meios de substância no que diz respeito a polaridade: polares e apolares. O termo "polar" nos dá a idéia de opostos, onde um dado ponto é negativo e o outro é positivo. Isso é resultado da diferença de contribuição na ligação entre elementos químicos diferentes. O mais eletronegativo atrai para perto de si o par de elétrons que estabelece a ligação com o outro átomo. Um exemplo de substância polar é água, considerada um solvente universal.
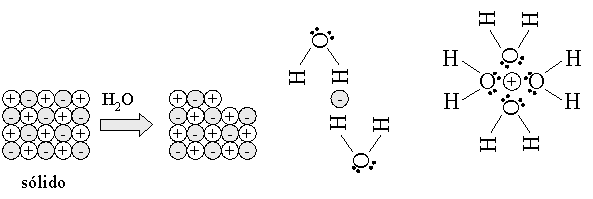
Substância iônica sofre um hidratação (água) ou solvatação (outro solvente)
A água é um excelente solvente polar para compostos orgânicos polares de baixo peso molecular, como o metanol, etanol, ácido fórmico, ácido acético, dentre outros. Possuindo um dipolo bastante acentuado, atrai por eletrostática o dipolo da outra molécula, de forma a potencializar a solubilização. Porém, essas moléculas orgânicas possuem uma parte polar, solúvel em água e uma parte apolar, insolúvel em água
A medida que aumenta-se o número de carbonos no grupo dos álcoois e ácidos carboxílicos por exemplo, a solubilidade, em meio aquoso vai diminuindo. É por isso que quando misturamos água com, por exemplo, butanol, constituído de 4 carbonos, a solubilidade em água diminui bastante, aparecendo claramente duas fases distintas indicando que as substâncias não são completamente miscíveis, mas sim parcialmente.
Exemplo
O etanol é miscível em qualquer proporção com a água devido as pontes de hidrogênio, já o decanol (álcool com 10 carbonos) é pouco solúvel, devido a sua estrutura possuir uma parte hidrofóbica, ou seja pouco polarizada.

Os químicos orgânicos definem usualmente um composto solúvel em água se pelo menos 3 g do composto se dissolvem em 100 ml de água (3% m/v).
Compostos que possuem grupos hidrofílicos seguem algumas regras:
1) compostos com 1 a 3 átomos de carbono são solúveis;
2) compostos com 4 a 5 átomos de carbono estão no limite da solubilidade;
3) Compostos com mais de 6 átomos são insolúveis.
Essas regras não se aplicam quando um composto contém mais de um grupo hidrofílico. Os polissacarídeos, as proteínas e os ácidos nucléicos contêm milhares de átomos de carbono e são todos solúveis. Porque eles possuem também milhares de grupos hidrofílicos.

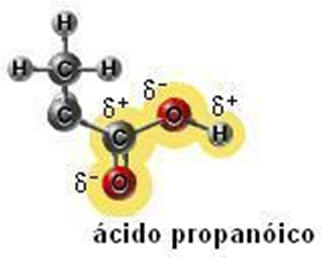
Vimos que a água é um ótimo solvente polar e, para compostos orgânicos polares de baixo peso molecular, também é um bom solvente. As ligações estabelecidas entre a água e o composto orgânico gera um fenômeno muito interessante, o qual pode ser realizado sem muitos equipamentos específicos de um laboratório. Podemos notar que tanto o etanol como o ácido propanóico possuem no mínimo uma ligação acentuadamente polar em suas moléculas, de forma a potencializar uma solubilidade em meio aquoso. No caso do álcool, a parte apolar não possui influência negativa na solubilidade em meio polar, já o ácido propanóico, com sua parte da molécula apolar, compromete a solubilidade total de composto em água. Mesmo assim, perceba que o número de pólos no ácido é maior do que no etanol.
HIDROCARBONETOS
|
Quanto maior o n.º de Carbonos maior o PM (peso molecular) , maior o PF (ponto de fusão) e PE (ponto de ebulição) ( maior a FVW). | |
|
Dois hidrocarbonetos de mesmo nº de C , quanto menos ramificada , maior a superfície de contato, maior a FVW, maior PF e PE. | |
|
Não são polares, não são solúveis em água ( ou são pouco solúveis), são solúveis em solventes orgânicos | |
|
São menos denso que a água. | |
|
PF e PE dos compostos cíclicos são maiores que dos não cíclicos. | |
|
PE e PF dos alcenos são maiores que dos alcanos correspondentes |
ÁLCOOIS
|
Formam pontes de Hidrogênio entre si (tem - OH) | |
|
Quanto maior o PM maior o PE ( maior a FVW). | |
|
PE (álcool) > PE (Hidrocarboneto correspondente) ( devido às pontes de Hidrogênio) | |
|
Quanto maior o PM , menor a solubilidade em água (os primeiros álcoois são solúveis em água pois são polares e formam pontes de Hidrogênio c/ a água). |
Exemplo
|
Álcool |
Fórmula |
Solubilidade (g/100g de H2O) |
|
Etanol |
CH3CH2OH |
Infinita |
|
1-propanol |
CH3CH2CH2OH |
Infinita |
|
1-butanol |
CH3CH2CH2CH2OH |
7,9 |
|
1-pentanol |
CH3CH2CH2CH2CH2OH |
2,3 |
|
1-octanol |
CH3CH2CH2CH2CH2CH2CH2CH2OH |
0,05 |
ÉTER
|
Não formam pontes de Hidrogênio entre si (só tem força dipolo-dipolo), por isso tem baixo PE e PF. | |
|
Quanto maior o PM, maior PE ( maior FVW). | |
|
Muito pouco solúveis em água (devido à força dipolo). | |
|
PE (álcool) > PE (éter) > PE (Hidrocarboneto de PM correspondente) |
ÁCIDOS CARBOXÍLICOS
|
( - COOH ) são polares (tem pontes de H entre si e com a água). | |
|
Os 4 primeiros ácidos são solúveis em água devido à polaridade e às pontes de H. | |
|
PE (ácidos) > PE (álcoois) > PE (aldeídos e cetonas) > PE (éter) > PE (Hidrocarboneto Correspondente). |
Exemplo
|
Ácido carboxílico |
Solubilidade (g/100g de H2O) |
|
Ácido acético |
Infinita |
|
Ácido pentanóico |
3,7 |
|
Ácido hexanóico |
1,0 |
|
Ácido heptanóico |
0,79 |
ALDEÍDOS E CETONAS
|
(C = O) são
polares (força dipolo-dipolo)
| |
|
Aldeídos e
Cetonas de baixo PM são solúveis em água (os outros são
insolúveis)
| |
|
PE (álcoois) > PE (aldeídos e cetonas) > PE (Hidrocarboneto Correspondente) ( pontes de H ) |
ÉSTER E CLORETOS ÁCIDOS
|
São compostos
polares (força dipolo)
| |
|
Tem PE próximos ao PE dos aldeídos e cetonas correspondentes |
AMINAS E AMIDAS
|
São polares pois formam pontes de H ( entre o N e o H ) , são solúveis em água |
6. DENSIDADE
As substâncias Orgânicas são, em geral pouco densas (tem densidade menor que da água) por este motivo quando insolúveis em água essas substâncias formam uma camada que “flutua” sobre a água, como acontece com a gasolina, o éter comum , o benzeno, etc.
Substâncias orgânicas contendo um ou mais átomos de massas atômicas elevadas podem ser mais densas que a água , exemplo CHBr3 é três vezes mais denso que a água.
7. VISCOSIDADE
Quanto maior a polaridade de uma molécula, maior será sua viscosidade.
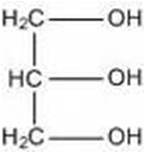
Comparando a gasolina e a glicerina:
 x
x
A glicerina apresenta:
|
Maior polaridade | |
|
Maior temperatura de ebulição | |
|
Maior solubilidade em água | |
|
Menor volatilidade | |
|
Maior viscosidade |
RESUMINDO TEMOS.....
A Polaridade de um composto orgânico depende da sua geometria e de suas ligações. É difícil determinar a geometria de uma molécula orgânica devido à presença de cadeias carbônicas. De um modo geral dizemos que:
- Hidrocarbonetos são apolares
- Presença de OH (ácidos, fenóis e álcoois) e NH (aminas) são muito polares devido às Pontes de Hidrogênio formadas.
- Em geral os demais compostos são polares, guardadas as devidas particularidades.
Moléculas Apolares se unem por forças de atração fracas conhecidas por vários nomes:
- Força de van der Waals
- Força de London
- Força dipolo induzido-dipolo instantâneo
- Dipolo induzido-dipolo induzido
Possuem baixo ponto de fusão e ebulição e são insolúveis em água.
Moléculas Polares se unem por dois tipos de força de atração distintas:
- Dipolo-dipolo ou dipolo permanente-dipolo permanente ou
- Ponte de hidrogênio (H – FON)
Possuem pontos de fusão e ebulição mais elevados e são solúveis em água.
Dentre essas forças, a mais forte é a Ponte de Hidrogênio, seguida pelo dipolo-dipolo e a força mais fraca é a de Van der Waals.
|
Maior
a temperatura de ebulição |
|
Maior
a energia necessária para a mudança de estado |
|
Maior
a força intermolecular (força de
atração) |

Fatores que influenciam no Ponto de Ebulição
|
Maior
massa |
|
Maior
temperatura de ebulição |
|
Para moléculas de mesma força
intermolecular |

|
Maior
número de interações ao longo da cadeia |
|
Maior
superfície |
|
Maior
a cadeia carbônica |
|
Maior
temperatura de ebulição |
|
Menor
número de interações ao longo da cadeia |
|
Menor
superfície |
|
Maior
número de ramificações |
|
Menor
temperatura de ebulição |
|
Para moléculas de mesma interação
intermolecular e mesma massa molar. |
 Cadeia carbônica
Cadeia carbônica
Com isso temos....
1) Para moléculas com tamanhos aproximadamente iguais, a TF e TE dependerá da interação (força) intermolecular.
2) Para moléculas com o mesmo tipo de interação, o Ponto de Fusão e o Ponto de Ebulição dependerá da massa molar.
3) Para moléculas de mesma interação e massa molar iguais (isômeros), a TF e TE dependerá do tipo da cadeia carbônica.
Solubilidade de compostos orgânicos
“Semelhante dissolve semelhante”
Água (H2O) e amônia (NH3) são polares.
Hidrocarbonetos, óleos e graxas são apolares.
Álcoois de até 3 carbonos possuem solubilidade infinita em água, pois são polares e interagem por pontes de hidrogênio.
ACIDEZ E BASICIDADE DE COMPOSTOS ORGÂNICOS
Caráter ácido
Segundo o conceito de Arrhenius, ácido é todo composto capaz de liberar o íon H+ em meio aquoso.
Existem duas funções orgânicas que possuem essa característica (por apresentarem o grupo hidroxila (OH)):
a) os ácidos carboxílicos
b) os fenóis
Apesar de os álcoois apresentarem o grupo OH eles podem ser considerados neutros.
Caráter básico
O único composto de caráter básico que nos interessa são as que pertencem ao grupo das aminas.