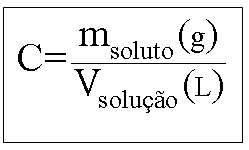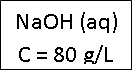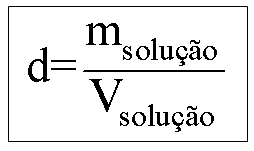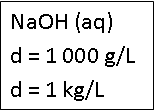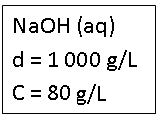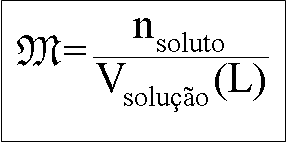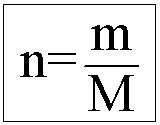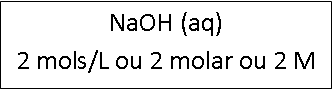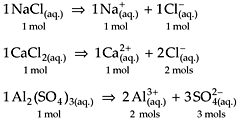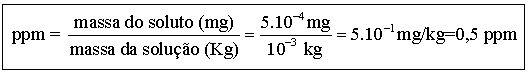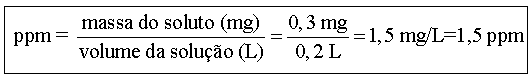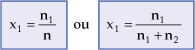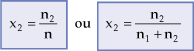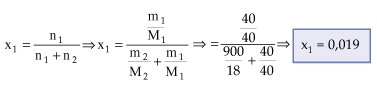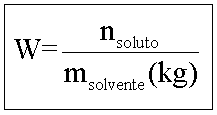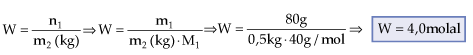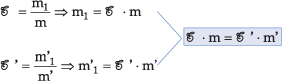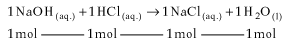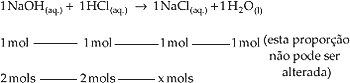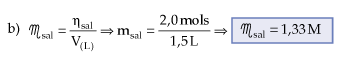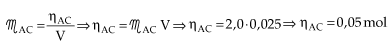Resumindo temos:

Lembrando que:
1 Å (angström) = 10 –7 mm
= 10 - 8 cm = 10 - 9 nm = 10
- 10 m
O ESTADO COLOIDAL
OS PRINCIPAIS TIPOS DE
DISPERSÕES COLOIDAIS
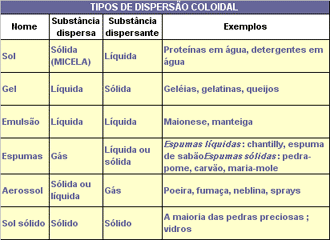
Como você perceberá , as
dispersões coloidais possuem participações importantes em nosso cotidiano,
sendo classificadas de acordo com o estado físico dos participantes. Vários
alimentos, medicamentos e produtos cosméticos são sistemas coloidais. Veja
alguns exemplos no quadro abaixo:
SAIBA MAIS SOBRE.....
UMA RECEITA DE GELATINA : COLÓIDES SOL E GEL
 A
receita que acompanha a embalagem de uma gelatina em pó descreve
o seguinte método de preparação:
A
receita que acompanha a embalagem de uma gelatina em pó descreve
o seguinte método de preparação:
- Despeje o conteúdo da embalagem em um recipiente.
- Adicione uma xícara (250 mL) de água fervente.
- Mexa até dissolver completamente.
- Adicione mais uma xícara de água fria ou gelada.
- Coloque o recipiente na geladeira.
Do ponto de vista químico, a gelatina em pó é uma mistura de
moléculas enormes, de grande massa molecular, denominadas
proteínas. E estas, por sua vez, são resultantes da união de
moléculas menores, denominadas aminoácidos.A hemoglobina, por
exemplo, que transporta oxigênio no sangue, possui cerca de 9 nm
de diâmetro e massa molecular igual a 64 500 u.
Como as moléculas de proteína apresentam um diâmetro situado
entre 1,0 nm e 1000 nm, dizemos que possuem dimensões coloidais.
Assim, o pó de gelatina, quando misturado em água aquecida,
constitui um colóide sol.
No entanto, o esfriamento final da gelatina na geladeira faz com
que as fibras de proteínas formem uma malha e passem a
constituir o que chamamos de colóide gel.
No gel, a fase dispersante forma uma complexa grade
tridimensional que mantém o disperso em uma estrutura
semi-rígida. Em alguns tipos de gel, essa estrutura pode ser
rompida por agitação. É o que ocorre, por exemplo, com algumas
tintas. Por agitação com o pincel, o gel transforma-se em sol.
Na parede, com o repouso, o gel volta a se reconstituir.
DE ONDE VEM A GELATINA?
 A
proteína mais abundante dos vertebrados é o colágeno, que
constitui aproximadamente 25% em massa das proteínas do corpo
humano. Parte dos ossos, tendões, dentes e pele é constituída de
colágeno.
A
proteína mais abundante dos vertebrados é o colágeno, que
constitui aproximadamente 25% em massa das proteínas do corpo
humano. Parte dos ossos, tendões, dentes e pele é constituída de
colágeno.
Apesar de o colágeno não ser comestível, seu aquecimento em água
fervente produz uma mistura de outras proteínas comestíveis,
denominadas genericamente de gelatinas. Tais proteínas são
usadas na fabricação de vários produtos, tais como filmes
fotográficos, colas, cápsulas de medicamentos e produtos
alimentícios.
As proteínas pertencem à classe dos colóides liófilos, ou seja,
aqueles que possuem afinidade com água. Como esses colóides têm
maior facilidade em transformar-se do estado gel para sol, ou
vice-versa, são chamados de reversíveis.
O CITOPLASMA: COLÓIDE OU SOLUÇÃO?
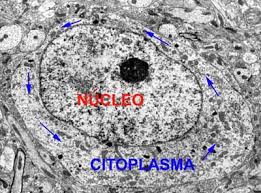 Você
provavelmente se lembra de que os orgânulos do citoplasma estão
mergulhados num material amorfo, viscoso, chamado hialoplasma.
Como componente majoritário, o hialoplasma contém, antes de mais
nada, muita água. Em segundo lugar, em termos de quantidade,
encontramos moléculas de proteínas.
Você
provavelmente se lembra de que os orgânulos do citoplasma estão
mergulhados num material amorfo, viscoso, chamado hialoplasma.
Como componente majoritário, o hialoplasma contém, antes de mais
nada, muita água. Em segundo lugar, em termos de quantidade,
encontramos moléculas de proteínas.
Neste sentido, podemos classificar o hialoplasma como sendo um
colóide, devido ao tamanho das macromoléculas protéicas. Por
outro lado, dissolvidas na água do hialoplasma, há uma grande
variedade de substâncias, com partículas de diâmetro inferior a
1 nm: sais minerais, gases da respiração, açúcares, aminoácidos,
ácidos graxos, nucleotídeos, etc. Se o critério de classificação
forem essas moléculas, você poderia dizer, sem dúvida, que o
hialoplasma é uma solução. Se você estiver considerando o
plasma, parte líquida do sangue, a situação é parecida: muita
água como dispersante, moléculas de proteínas, principalmente
albumina, sais minerais, açúcares, ácidos graxos, vitaminas,
gases respiratórios. Dessa forma, o plasma sangüíneo é um
colóide e, ao mesmo tempo, uma solução.
OS
COLÓIDES E O MOVIMENTO AMEBÓIDE
 A
região de hialoplasma mais externa da célula, logo abaixo da
membrana plasmática, também dita ectoplasma, é um colóide no
estado de gel. Já a maior parte do hialoplasma, interna, chamada
endoplasma, é um colóide no estado de sol. È bastante antiga a
observação de que células vivas, como amebas e leucócitos, têm a
capacidade de transformar, em certas circunstâncias, partes do
hialoplasma geleificadas em sol, e vice-versa. Essas
transformações estão na base do famoso movimento amebóide,
através do qual amebas e leucócitos "derramam" seu citoplasma
para a frente, formando pseudópodes. Os pseudópodes, vamos
lembrar, não apenas permitem a locomoção da célula, como também
sua nutrição, pelo conhecido processo da fagocitose.
A
região de hialoplasma mais externa da célula, logo abaixo da
membrana plasmática, também dita ectoplasma, é um colóide no
estado de gel. Já a maior parte do hialoplasma, interna, chamada
endoplasma, é um colóide no estado de sol. È bastante antiga a
observação de que células vivas, como amebas e leucócitos, têm a
capacidade de transformar, em certas circunstâncias, partes do
hialoplasma geleificadas em sol, e vice-versa. Essas
transformações estão na base do famoso movimento amebóide,
através do qual amebas e leucócitos "derramam" seu citoplasma
para a frente, formando pseudópodes. Os pseudópodes, vamos
lembrar, não apenas permitem a locomoção da célula, como também
sua nutrição, pelo conhecido processo da fagocitose.
Não se sabe ainda, ao certo, os mecanismos que levam o
hialoplasma da ameba a se transformar e fluir para formar os
pseudópodes. Há fortes indícios, no entanto, de que finíssimos
filamentos de uma proteína chamada actina, presentes no
hialoplasma estejam relacionados com esse fluxo citoplasmático,
fundamental para a formação de pseudópodes. Uma observação: a
actina de que estamos falando é a mesma substância que, em
conjunto com a miosina, forma o complexo contrátil das células
musculares.
AS
EMULSÕES: COMO SE FAZ MAIONESE?
 Todos
sabemos que água e óleo não se misturam e isso habitualmente é
justificado pelo fato da água ser um líquido polar, enquanto o
óleo é formado por moléculas praticamente apolares.
Todos
sabemos que água e óleo não se misturam e isso habitualmente é
justificado pelo fato da água ser um líquido polar, enquanto o
óleo é formado por moléculas praticamente apolares.
Se você agitar uma mistura de água e óleo em um liquidificador,
gotas de óleo, de dimensões coloidais, ficarão espalhadas na
água por algum tempo. A esse sistema chamamos de emulsão.
Note que, após alguns minutos, as gotas de óleo aglutinam-se e a
fase oleosa é reconstituída, voltando a flutuar sobre a água.
Isto significa que a emulsão formada era instável.
Você sabe como se faz maionese?
 Para
fazer maionese, basta colocar uma gema do ovo em um
liquidificador, bater vigorosamente e acrescentar um pouco de
óleo. Forma-se, assim, uma emulsão estável.
Para
fazer maionese, basta colocar uma gema do ovo em um
liquidificador, bater vigorosamente e acrescentar um pouco de
óleo. Forma-se, assim, uma emulsão estável.
Mas como isso acontece? Como o óleo e a água podem ser
misturados?
A razão fundamental está na presença das proteínas da gema.
As moléculas de proteína envolvem as gotas de óleo, formando uma
película hidrófila, ou seja, que possui afinidade com a água. A
essas proteínas chamamos de colóides protetores ou agentes
emulsificantes ou tensoativos.
(Obs.: Muitas vezes, o mesmo sistema se enquadra em várias
classificações. O leite, por exemplo, é uma solução aquosa de
sais e açúcares; um colóide sol em relação às proteínas e uma
emulsão em relação às gorduras. No leite, o agente emulsificante
é uma proteína chamada caseína. Além disso, algumas partículas
de gordura, grandes o suficiente para serem vistas ao
microscópio comum, estão em suspensão.)
O QUE SÃO TENSOATIVOS
Os
tensoativos são responsáveis pela característica mais importante
e desejada em um detergente, a capacidade de remoção das
sujidades e também de permitir a miscibilidade de um óleo na
água. Este fato é possível devido a sua estrutura, que possui
uma parte hidrofílica e uma parte hidrofóbica.
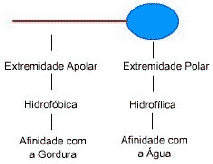 A
figura ao lado representa esquematicamente a estrutura de um
tensoativo. Eles reduzem a tensão superficial da água,
permitindo que a sujeira possa ser removida facilmente ou mesmo
que um óleo possa se misturar com a água, através da formação de
micelas.
A
figura ao lado representa esquematicamente a estrutura de um
tensoativo. Eles reduzem a tensão superficial da água,
permitindo que a sujeira possa ser removida facilmente ou mesmo
que um óleo possa se misturar com a água, através da formação de
micelas.
Numa micela, a extremidade apolar do tensoativo fica voltada
para o centro, interagindo com o óleo (ou substâncias
hidrofóbicas) enquanto a extremidade polar para fora
(interagindo com a água).
As micelas são estruturas geralmente esféricas, de natureza
coloidal, formadas de tal modo que as partes não polares do
detergente se orientam para o interior da mesma, criando assim,
uma superfície iônica. Podemos dizer que as soluções de
tensoativos formam sistemas dinâmicos onde as micelas estão
continuamente sendo formadas e destruídas. Essa característica
das soluções de detergentes é importante para o processo de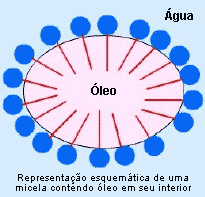 remoção das sujidades, que envolve o deslocamento das partículas
de sujeiras de natureza lipofílica para o interior das micelas e
a estabilização das mesmas de modo a mantê-las em suspensão,
evitando que a sujeira volte a depositar-se sobre a superfície
que está sendo limpa.
remoção das sujidades, que envolve o deslocamento das partículas
de sujeiras de natureza lipofílica para o interior das micelas e
a estabilização das mesmas de modo a mantê-las em suspensão,
evitando que a sujeira volte a depositar-se sobre a superfície
que está sendo limpa.
Os tensoativos são divididos em aniônicos, catiônicos, anfóteros
e não iônicos.
A associação de alguns deles pode, além de outras coisas,
melhorar o poder de limpeza do detergente e diminuir sua
irritabilidade, ou seja, aumentar sua suavidade.
Exemplos: Lauril, proteínas, etc.
De um modo geral, na grande maioria dos casos, podemos dizer que
um tensoativo apresenta ao mesmo tempo características de agente
molhante, de agente emulsionante, de detergente e de espumante.
Entretanto, uma destas características é sempre mais marcante em
um determinado tensoativo do que as demais. É esta
característica dominante que determina a sua classificação como
detergente, emulsionante, etc., conforme o caso.
O EFEITO TYNDALL
Se colocarmos lado a lado um copo com solução aquosa de
açúcar e outro copo com leite diluído em água, o feixe de uma
caneta laser deixará um rastro somente no copo que contém uma
dispersão coloidal de gelatina em água.
Este fenômeno, conhecido como efeito Tyndall, ocorre devido à
dispersão da luz pelas partículas coloidais. No béquer contendo
uma solução de açúcar em água, as moléculas do soluto não são
suficientemente grandes para dispersarem a luz.

Efeito de Tyndall:
Os colóides dispersam fortemente a luz, pois as partículas
dispersas têm tamanhos semelhantes ao comprimento de onda da luz
visível. Este fenômeno é chamado efeito de
Tyndall e permite distinguir as soluções verdadeiras
dos colóides, pois as soluções verdadeiras são transparentes, ou
seja não dispersam a luz
O efeito Tyndall recebeu
esse nome , em homenagem ao brilhante físico inglês, John
Tyndall (1820 – 1893), que demonstrou por que o céu é azul, e
estudou de forma muito completa os fenômenos de espalhamento da
luz por partículas e poeira. Esse efeito também foi observado
por Tyndall quando um pincel de luz atravessava alguns sistemas
coloidais. Esse espalhamento da luz é seletivo, isto é, depende
das dimensões das partículas dispersas e do comprimento de onda
da radiação. Dessa forma, é possível que uma determinada cor de
luz se manifeste de maneira mais acentuada do que outras.
AEROSSÓIS
 O
ambiente em que vivemos precisa ser limpo com regularidade, para
que que seja retirada a poeira que constantemente é depositada
sobre os objetos.
O
ambiente em que vivemos precisa ser limpo com regularidade, para
que que seja retirada a poeira que constantemente é depositada
sobre os objetos.
Esses grãos de poeira, de diâmetros superiores a 1 000 nm, estão
em suspensão e tendem a sedimentar. No entanto, há no ar alguns
grãos de poeira de dimensões coloidais que nunca sedimentam.
Esses tipo de colóide chama-se aerossol.
 Neblinas , fumaças e
sprays são outros exemplos de aerossóis do cotidiano. Quando
observamos o rastro luminoso deixado pela luz de um projetor de
slides em uma sala escura, ou quando notamos os feixes luminosos
dos faróis dos carros em dias com forte neblina, devemos nos
lembrar do efeito Tyndall que a luz pode provocar quando atinge
partículas coloidais sólidas existentes no ar.
Neblinas , fumaças e
sprays são outros exemplos de aerossóis do cotidiano. Quando
observamos o rastro luminoso deixado pela luz de um projetor de
slides em uma sala escura, ou quando notamos os feixes luminosos
dos faróis dos carros em dias com forte neblina, devemos nos
lembrar do efeito Tyndall que a luz pode provocar quando atinge
partículas coloidais sólidas existentes no ar.
ESPUMAS
 Quando
um gás é borbulhado em um líquido, além das bolhas enormes e
visíveis, são formadas também bolhas de dimensões coloidais. Por
isso, as espumas também podem ser classificadas como colóides.
Um bom exemplo é o chantilly, formado pela mistura de ar em
creme de leite. Um sólido que possui poros de dimensões
coloidais é classificado como espuma sólida. É o caso, por
exemplo, da pedra-pome, que possui ar em microscópicos poros de
dimensões coloidais.
Quando
um gás é borbulhado em um líquido, além das bolhas enormes e
visíveis, são formadas também bolhas de dimensões coloidais. Por
isso, as espumas também podem ser classificadas como colóides.
Um bom exemplo é o chantilly, formado pela mistura de ar em
creme de leite. Um sólido que possui poros de dimensões
coloidais é classificado como espuma sólida. É o caso, por
exemplo, da pedra-pome, que possui ar em microscópicos poros de
dimensões coloidais.
Como você percebeu através destas rápidas informações, o vasto
campo dos sistemas coloidais é atraente e gerador de muitas
atividades profissionais. No mundo, as industrias ligadas aos
colóides empregam milhões de pessoas e movimentam muitos bilhões
de dólares.
Para ler mais:
Biologia, de Sezar Sasson e César S.Júnior (Ed. Saraiva)
Química- Realidade e Contexto, de A. Lembo (Ed. Ática)
Fundamentos de Química Geral, de Morris Hein e Susan Arena
(Ed.Livros Técnicos e Científicos)
SOLUÇÕES
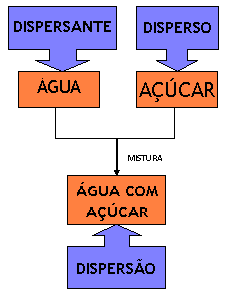
São misturas homogêneas de duas ou mais substâncias.
Nas soluções a fase dispersa recebe o nome de soluto
e o dispersante de solvente.
Existem vários tipos de solventes, porém, só iremos
considerar soluções nas quais o solvente é a água (solvente universal),
denominadas de soluções aquosas.
CLASSIFICAÇÃO DAS SOLUÇÕES
DE ACORDO COM O ESTADO FÍSICO
SOLUÇÃO SÓLIDA
O solvente é
sempre sólido e o soluto pode ser: sólido, líquido ou gasoso.

Estátua em Bronze do século V a.C.: solução sólida (liga metálica de cobre e
estanho)
Exemplos: ligas
metálicas (Solda: Sn+Pb, Ouro 18K: Au+Ag e/ou Cu, Bronze: Cu+Sn, Aço: Fe+C,
Latão: Cu+Zn, Amálgama: Hg+Ag, etc.)
SOLUÇÃO LÍQUIDA
O solvente é
sempre líquido e o soluto pode ser: sólido, líquido ou gasoso.

Refrigerante: solução líquida com solvente líquido e soluto gasoso
Exemplos: soro
fisiológico (água - solvente, sal - soluto), refrigerantes (água - solvente,
gás carbônico - soluto), álcool hidratado (água - solvente, álcool - soluto)
SOLUÇÃO GASOSA
O solvente é
gasoso e o soluto gasoso.

Gás de cozinha: solução gasosa com mistura de gases propano e butano.
Exemplo: ar
atmosférico filtrado
DE ACORDO COM A NATUREZA DO SOLUTO
SOLUÇÃO MOLECULAR
As partículas
dispersas do soluto são moléculas. A solução molecular é também chamada de
solução não-eletrolítica.
Exemplo: água +
açúcar (C6H12O6).
SOLUÇÃO IÔNICA
As partículas
dispersas do soluto são íons ou íons e moléculas (dependendo do sal ou do
ácido).
Exemplo: água +
sal (NaCl), água + ácido clorídrico (HCl)
Esquematicamente temos:

DE ACORDO COM A PROPORÇÃO DO SOLUTO EM RELAÇÃO AO SOLVENTE
Num determinado dia, ao receber visitas em sua casa, você
resolve preparar suco de laranja e suco de uva para servir a seus
convidados. Ao servir o suco de laranja, nota-se que algumas pessoas fazem
cara feia e dizem: nossa como está forte! Enquanto que outras pessoas que
beberam suco de uva dizem: Hum, este está muito fraco!
Nestes dois casos descritos acima, podemos observar que
temos dois tipos de soluções: diluída e concentrada.
DILUÍDA
Pouco soluto dissolvido em relação ao solvente (suco de
uva).
CONCENTRADA
Muito soluto dissolvido em relação ao solvente (suco de
laranja).
Ao juntarmos, gradativamente, açúcar e água em temperatura
constante e sob agitação contínua, notamos que o sólido se dissolve, até não
poder ser mais visto. Vamos acrescentando mais açúcar e tornando a solução
mais concentrada, até que em um dado momento, o açúcar não se dissolve mais
na água, mas se deposita no fundo ou se precipita ou se deposita ou se
decanta. Neste momento, dizemos que a solução está saturada e
apresenta um corpo de fundo.
SATURADA
Solução que contém uma quantidade máxima de soluto
dissolvido no solvente numa determinada temperatura e pressão.
Esta quantidade máxima de soluto dissolvido é expresso
através do coeficiente de solubilidade (CS).
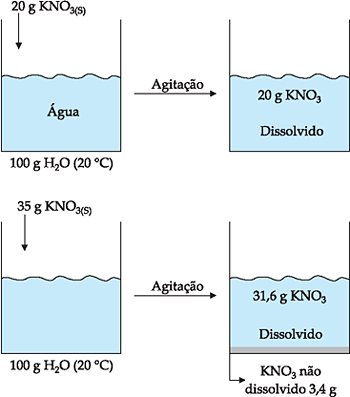
Por exemplo, a 20 °C, a solubilidade
do KNO3
é 31,6 g em cada 100 g de H2O.
Isto significa que podemos dissolver até 31,6 g de KNO3
a 20 °C em 100 g de H2O.
A variação de temperatura pode alterar o coeficiente de
solubilidade de uma substância. Geralmente, o aumento da temperatura aumenta
a solubilidade da maioria das substâncias.
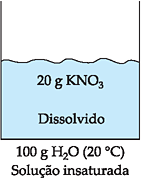
INSATURADA OU NÃO SATURADA
Ocorre quando a quantidade de soluto
adicionada é inferior ao coeficiente de solubilidade. Por exemplo, o
coeficiente de solubilidade do KNO3
em água a 20 °C é 31,6 g/100 g H2O,
portanto, a adição de qualquer quantidade de KNO3
abaixo de 31,6 g em 100 g de água, a 20 °C, produz solução insaturada
SUPERSATURADA
Solução que contém uma quantidade de soluto dissolvido
superior à solução saturada por meio de uma variação de temperatura.
Por exemplo: a 40 °C, a solubilidade
do KNO3
é 61,47 g/100 g H2O
e, a 20 °C, é 31,6 g/100 g H2O.
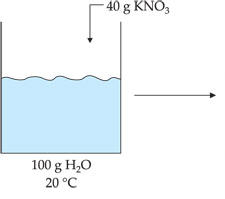
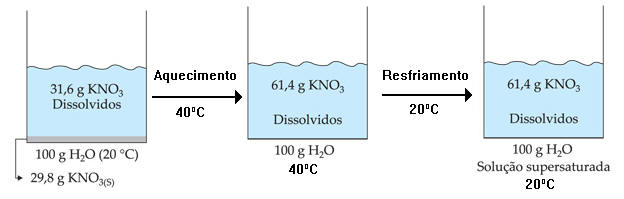
As soluções supersaturadas são
instáveis, ou seja, qualquer perturbação no meio irá fazer com que o KNO3
precipite, tornando o sistema heterogêneo.
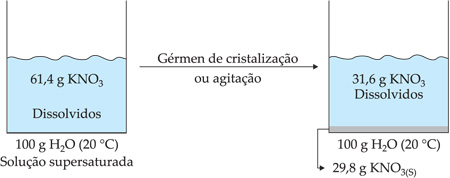
Resumindo temos:
Solubilidade de Gases em Líquidos
Normalmente, os gases são pouco solúveis nos líquidos.
Dois fatores alteram consideravelmente a solubilidade:
Temperatura
 Todo
aumento de temperatura diminui a solubilidade do gás no líquido – Por
exemplo, para eliminar gases dissolvidos na água, é feito o aquecimento por
um certo período de tempo. Sendo assim, a diminuição da temperatura facilita
a solubilidade de um gás num líquido - Por exemplo, na piracema os peixes
nadam contra a corrente para realizar a desova nas nascentes onde as águas
são mais oxigenadas, portanto, facilitando a reprodução e desova.
Todo
aumento de temperatura diminui a solubilidade do gás no líquido – Por
exemplo, para eliminar gases dissolvidos na água, é feito o aquecimento por
um certo período de tempo. Sendo assim, a diminuição da temperatura facilita
a solubilidade de um gás num líquido - Por exemplo, na piracema os peixes
nadam contra a corrente para realizar a desova nas nascentes onde as águas
são mais oxigenadas, portanto, facilitando a reprodução e desova.
Pressão
Quando não ocorre reação do gás com o
líquido, a influência da pressão é estabelecida pela lei de Henry:
"Em temperatura constante, a
solubilidade de um gás num líquido é diretamente proporcional à pressão".

Por exemplo, podemos citar os
refrigerantes, que apresentam grande quantidade de CO2
dissolvido sob pressão. Quando o refrigerante é aberto, a pressão diminui,
fazendo com que o excesso de CO2
dissolvido no refrigerante escape.
Curvas de Solubilidade
São diagramas que mostram a
variação dos coeficientes de solubilidade das substâncias em função da
temperatura.
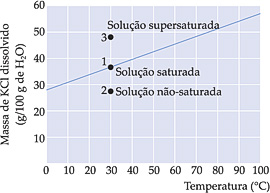
Analisando o gráfico, observamos que regiões abaixo da
curva representam solução não-saturada, sobre a curva, região saturada e
acima da curva, desde que as quantidades permaneçam em solução, região
supersaturada.
O gráfico abaixo representa a solubilidade de várias
substâncias em função da temperatura.
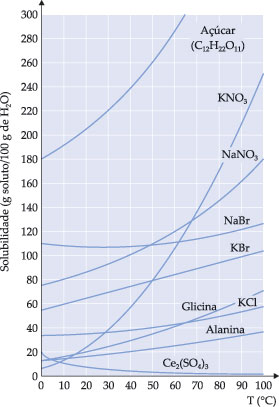
Observamos que a maioria das
substâncias aumenta a solubilidade com o aumento da temperatura. Podemos
dizer, então, que se trata de uma dissolução endotérmica.
Para uma substância como Ce2(SO4)3,
a solubilidade diminui com o aumento da temperatura; portanto, trata-se de
uma dissolução exotérmica.
O gráfico do coeficiente de
solubilidade em função da temperatura é utilizado principalmente para
informar a solubilidade de uma ou várias substâncias em função da
temperatura. Por exemplo:
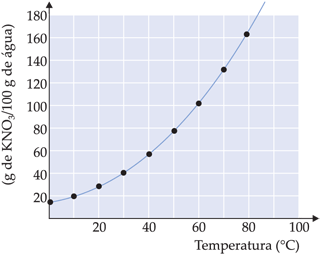
Interpretando o gráfico:
– na temperatura de 50°C, a quantidade
máxima de KNO3
que se dissolve em 100 g de água são 80
g. A solução em questão é saturada;
– para obtermos uma solução saturada
KNO3
a 40°C, basta dissolver 60 g de KNO3
em 100 g de água;
– se resfriarmos uma solução saturada
de 50°C para 40°C, teremos um corpo de fundo igual a 20 g de KNO3;
– 200 g de água a 40°C dissolvem no
máximo 120 g de KNO3.
PREPARANDO UMA SOLUÇÃO
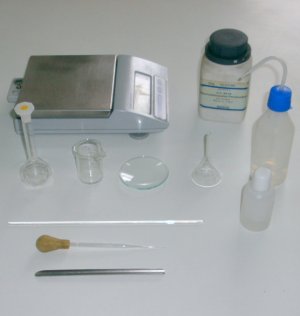
Materiais utilizados no preparo da solução.
Para prepararmos uma solução de 80 g de NaOH em 1 litro de
solução, seguiremos o seguinte
roteiro:
1) Medir a massa do soluto (80 g de NaOH);

2) Transferir o soluto para um béquer e adicionar água
destilada em quantidade suficiente para dissolver o soluto;



3) Transferir o soluto dissolvido para o balão volumétrico
e homogeneizar a solução invertendo o balão tapado várias vezes;

4) Completa-se o volume da solução até a marca do balão
volumétrico e homogeneizar.



IDENTIFICANDO A SOLUÇÃO
Depois de preparar a solução devemos
transferir a solução para o frasco,
previamente rotulado com uma etiqueta, indicando o nome da solução, a sua
concentração e a data de preparação.
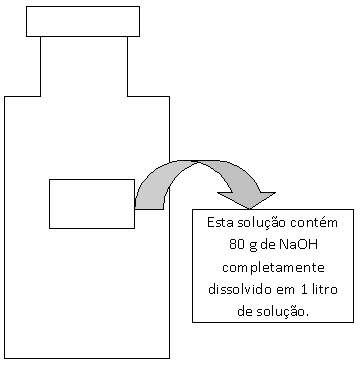
Mas observe que as informações referentes à solução não cabem
no rótulo, portanto, neste caso devemos codificar as informações
através de relações matemáticas simplificadas denominadas de
concentrações das soluções.
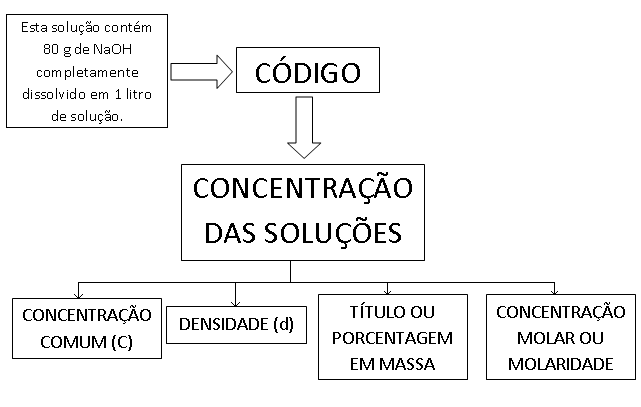
Concentração Comum (C)
Indica a relação da massa do soluto em gramas pelo volume
da solução em litros.
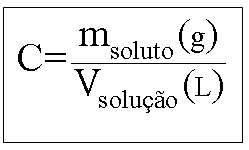
No exemplo ilustrado acima, codificando as informações da
solução teríamos:
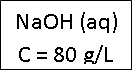
Interpretação:
Esta solução contém 80 g de NaOH dissolvido em qsp (quantidade
suficiente para) 1 litro de solução.
Densidade (d)
Indica a relação da massa da solução pelo volume por ela
ocupado.
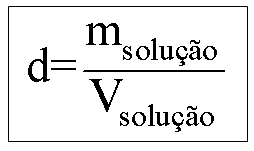
No exemplo ilustrado acima, codificando as informações da
solução teríamos:
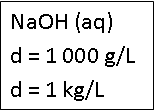
Interpretação:
Cada 1 litro da solução de NaOH possui massa de 1000 g ou
1 kg.
Observação
Não confunda Concentração Comum (C) e densidade
(d).
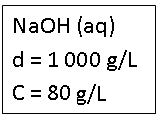
Soluto: NaOH = 80 g
Solvente: H2O = 920 g
Solução: NaOH (aq) = 1000 g
Interpretação
d = 1000 g/L → cada 1 litro da solução
de NaOH possui massa de 1000 g.
C = 80 g/L → cada 1 litro de solução possui
80 g de NaOH dissolvido.
Concentração Molar ou Molaridade
Indica a relação do número de mols do soluto,
pelo volume da solução em litros.
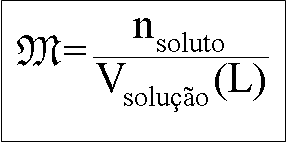
Sendo que:
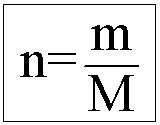
Onde: n = número de mols, m = massa em gramas, M = massa
molar (g/mol)
No exemplo ilustrado acima, codificando as informações da
solução teríamos:
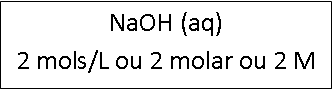
Interpretação:
Cada 1 litro da solução possui 2 mols de NaOH dissolvido.
(Dado: NaOH - M = 40g/mol)
Concentração Molar para Soluções Iônicas
Monta-se a equação da dissociação do
eletrólito (soluto) e, em seguida, verifica-se a quantidade em mols do
cátion e do ânion produzidos para cada mol do soluto. Assim, teremos uma
relação em mol/L entre o soluto e os íons produzidos. Observe os exemplos a
seguir:
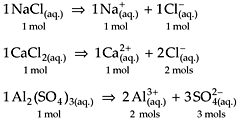
PORCENTAGEM EM MASSA OU TÍTULO
Indica a relação da massa do soluto pela massa da solução,
ou ainda, a porcentagem em massa do soluto na massa da solução.

No exemplo ilustrado acima, codificando as informações da
solução teríamos:
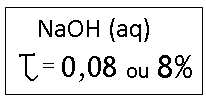
Interpretação:
Da massa total da solução 8% corresponde à massa do
soluto.
Exemplos

No rótulo de um frasco de soro fisiológico à 0,9 % interpretamos da seguinte
maneira: em 100 mL do soro fisiológico temos 0,9 g de NaCl.


Vodka 40% volume ou 40oGL: 100 mL da bebida possui 40% em volume
ou 40 mL de álcool etílico

Cerveja 5,2% volume ou 5,2oGL: 100 mL da bebida possui 5,2% em
volume ou 5,2 mL de álcool etílico
A
água oxigenada 10 vol ou 20 vol é uma solução aquosa que à temperatura
ambiente sofre decomposição:
H2O2(aq)
→ H2O(l) + O2(g)
Devido a liberação do oxigênio, esta
solução é utilizada como antisséptico na limpeza de ferimentos, pois o
oxigênio liberado elimina as bactérias aeróbicas, que causam o apodrecimento
do tecido.
Água oxigenada é utilizado como antisséptico na limpeza de feridas.

Água oxigenada 10 volumes utilizado para desinfecção de ferimentos: 1 cm3
H2O2(aq) produz 10 cm3 de O2(g)
nas CNTP

Água oxigenada 20 volumes utilizado para descolorir cabelos: 1 cm3
H2O2(aq) produz 20 cm3 de O2(g)
nas CNTP
Saiba mais sobre....
CÓDIGO NACIONAL DE TRÂNSITO
Em 19 de junho de 2008
foi aprovada a Lei 11.705, modificando o Código de Trânsito
Brasileiro. Apelidada de "lei seca", proíbe o consumo da
quantidade de bebida alcoólica superior a 0,1 mg de álcool
por litro de ar expelido dos pulmões no exame do bafômetro
(ou 2 dg de álcool por litro de sangue) por condutores de
veículos, ficando o condutor transgressor sujeito a pena de
multa, a suspensão da carteira de habilitação por 12 meses e
até a pena de detenção, dependendo da concentração de álcool
por litro de sangue.
Apesar de não ser
permitida nenhuma concentração de álcool, existem valores
fixos, prevendo casos excepcionais, tais como medicamentos à
base de álcool e erro do aparelho que faz o teste. A
concentração permitida no Brasil é de 0,2 g de álcool por
litro de sangue, ou, 0,1 mg de álcool por litro de ar
expelido dos pulmões no exame do bafômetro.
Essa equivalência (sangue e ar) é em decorrência da Lei
de Henry, acerca das trocas entre um gás, um vapor
(álcool) e um líquido (sangue), sendo que existe uma relação
constante entre a quantidade de álcool existente no sangue e
no ar alveolar, sendo essa constante de 1/2000. Assim, 1 cm3
de sangue contém tanto álcool quanto 2000 cm3 de
ar alveolar.
O entendimento dessa relação de equivalência é de suma
importância, especialmente considerando-se que uma das
formas que nossas autoridades utilizam para comprovar a
infração é por meio do "bafômetro". Deve o agente da
autoridade de trânsito tomar cautela em saber qual a unidade
que o resultado do exame o está informando. Nos
bafômetros o resultado
obtido é em %BAC (Blood Alcohol Concentrations) , que
é numericamente o mesmo que a quantidade do álcool no sangue
e não no ar alveolar.
Para exemplificar melhor, o resultado no bafômetro de 0,08
BAC significa 8 decigramas por litro de sangue ou 0,4 mg por
litro de ar alveolar, ou ainda, 1mL por litro de sangue,
pela densidade do álcool ser um pouco inferior ao da água
(1mL de água = 1g de água). Em recente reportagem do Jornal
Folha de São Paulo foi relatado o caso de uma jovem
estudante detida e encaminhada para a delegacia de polícia
pela condução de veículo sob influência de álcool. Mais
tarde comprovou-se que na verdade ela estava exatamente na
metade do limite estabelecido pelo CTB. Quem sabe o erro
cometido pelo agente policial não reside no desconhecimento
de tais equivalências?
Metabolismo do álcool
O metabolismo no fígado remove de 90% a 98%
da droga circulante. O resto é eliminado pelos rins, pulmões
e pele.
Um adulto de 70kg consegue metabolizar de 5 a
10 gramas de álcool por hora. Como um drinque contém, em
média, de 12 a 15 gramas, a droga acumula-se
progressivamente no organismo, mesmo em quem bebe apenas um
drinque por hora.
O álcool que cai na circulação sofre um
processo químico chamado oxidação que o decompõe em gás
carbônico (CO2) e água. Como nesse processo
ocorre liberação de energia, os médicos recomendam evitar
bebidas alcoólicas aos que desejam emagrecer, uma vez que
cada grama de álcool ingerido produz 7,1 kcal, valor
expressivo diante das 8 kcal por grama de gordura e das 4
kcal por grama de açúcar ou proteína.
Porque é aplicada uma injeção
de glicose (C6H12O6)
em pessoas embriagadas?
O etanol ou alcool etílico, o principal
componente das bebidas alcoólicas, é
absorvido a partir do intestino delgado e
transportado diretamente para o fígado, onde
é metabolizado por reações de oxidação que
interferem na síntese de glicose pela
gliconeogenese ( o ciclo metabólico de
conversão para glicose no organismo, que a
usa como fonte de energia).
A ingestão excessiva de etanol desvia os
intermediários da gliconeogenese para rotas
alternativas de reação, resultando em
síntese diminuída de glicose. Isso acarreta
hipoglicemia (queda da taxa de açúcar no
sangue). A hipoglicemia pode produzir muitos
dos comportamentos associados à intoxicação
alcoólica – agitação, julgamento diminuído,
etc...
Em um curto período (8 a 12 horas) após a
ingestão de grande quantidade de álcool pode
ocorrer a ressaca, que se caracteriza por
dor de cabeça, náusea, tremores e vômitos.
Isso ocorre porque o metabolismo do álcool
etílico gera, em uma de suas etapas, o
aldeído acético que quando se acumula no
organismo, é o responsável por sensações de
desconforto.
A concentração de álcool no sangue depende
de fatores como o volume consumido em um
determinado tempo, a massa corporal, o
metabolismo de quem bebe e a quantidade de
comida no estomago. Quando o álcool já está
no sangue, não há comida ou bebida que
interfira em seus efeitos. Os sintomas que
se observam são mostrados a seguir e a
quantidade ingerida é diferente na mulher
por conta da absorção maior e da quantidade
de gordura corporal, proporcionalmente maior
que no homem, o que aumenta a
biodisponibilidade do álcool:
“Se bebeu não dirija,
se dirigir não beba “
|
Concentração de
álcool no sangue(g/l) |
Efeito |
|
Até 0,16 |
Nenhum
efeito aparente |
|
0,200 a 0,30 |
Falsa estimativa
de distância e de velocidade |
|
0,30 a 0,50 |
Começo de risco
de acidente |
|
0,50 a 0,80 |
Euforia do
condutor, risco de acidente
multiplicado
por quatro |
|
1,50 a 3,00 |
Visão
dupla, condução perigosíssima |
|
3,00 a 5,00 |
Embriaguez
profunda, condução impossível |
|
Mais que 5,00 |
Coma, podendo
levar a morte |
Efeitos
do alcool em um
individuo, em função da
concentração no sangue
ROTEIRO PARA RESOLUÇÃO DOS PROBLEMAS ENVOLVENDO
CONCENTRAÇÃO DAS SOLUÇÕES
A resolução dos problemas, sem a utilização de fórmulas,
segue as seguintes etapas:
1º) Transformar a unidade de concentração em regra de
três.
Obs.: Se o problema pedir para calcular a concentração,
coloca-se o padrão de volume que é sempre 1 litro.
2º) Colocar o dado e a pergunta do problema.
Obs.: Não esqueça de uniformizar as unidades.
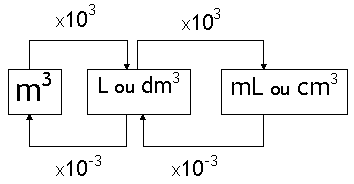
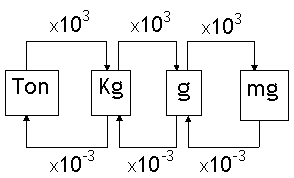
3º) Calcular o valor da incógnita.
Exemplos
01) Calcular a concentração em g/L de uma solução com 40 g
de soluto em 500 cm3 de solução.
Dados:
Massa do soluto = 40 g
Volume da solução = 500 cm3 = 0,5
L
Concentração da solução = ? (g/L)
RESOLUÇÃO
40 g de soluto ------------------ 0,5 L de
solução
X ------------------ 1,0 L
de solução
X = 80 g de soluto
Desta
forma
ficamos com: C = 80 g/L
02) Calcular a massa de soluto dissolvido em 250 mL de
solução com concentração de 4 g/L.
Dados:
Massa do soluto = ? (g)
Volume da solução = 250 mL = 0,25 L
Concentração da solução = 4 g/L
RESOLUÇÃO
4 g de soluto ------------------ 1,0 L de
solução
X ------------------ 0,25
L de solução
X = 1 g de soluto
03) Um copo contém 115 mL de álcool etílico cuja densidade
é 800 g/L. Qual a massa de álcool contida no copo?
Dados:
Massa álcool = ? (g)
Volume do álcool = 115 mL = 0,115 L
Densidade do álcool = 800 g/L
RESOLUÇÃO
800 g de álcool ------------------ 1,0 L de
álcool
X ------------------ 0,115 L de álcool
X = 92 g de álcool
04) Uma solução foi preparada misturando-se 20 g de um sal
em 200 mL de água (d =1 g/mL), originado uma solução cujo volume é 250 mL.
Determine a densidade da solução em g/L.
Dados:
Massa do soluto = 20 g
Volume do solvente = 200 mL
Massa do solvente = 200 g (pois a água possui
d = 1 g/mL)
Com isso ficamos com: Massa da solução = 220
g (massa do soluto + massa do solvente)
Volume da solução = 250 mL = 0,25 L
Densidade da solução = ? (g/L)
RESOLUÇÃO
220 g de solução ------------------ 0,25 L de
solução
X ------------------
1,0 L de solução
X = 880 g de solução
Desta forma ficamos com: d = 880 g/L
05) Certo produto para limpar forno é uma solução aquosa 0,5
M de NaOH. Qual a massa do NaOH contida em 800 mL do produto? (Dado: NaOH
→ M = 40 g/mol)
Dados:
Massa do soluto = ? (g)
NaOH
à
M = 40 g/mol
Volume da solução = 800 mL = 0,8 L
Concentração Molar = 0,5 M = 0,5 mol/L
RESOLUÇÃO
1º) Determinar a massa do soluto em 1 L:
1 mol de NaOH ------------------ 40g
0,5 mol de NaOH ------------------ X
X = 20 g
2º) Determinar a massa do soluto em 0,8 L:
20 g de NaOH ------------------- 1,0 L de solução
X ------------------- 0,8 L de solução
X = 16 g de NaOH
06) 136,8 g de Al2(SO4)3
foram dissolvidos em água suficiente para 800 mL de solução. Determine a
concentração em mols/L da solução obtida. (Dado:
Al2(SO4)3
→ M = 342 g/mol)
Dados:
Massa do soluto = 136,8 g
Al2(SO4)3
à
M = 342 g/mol
Volume da solução = 800 mL = 0,8 L
Concentração Molar = ? (mol/L)
RESOLUÇÃO
1º) Determinar o número de mols do soluto em 0,8 L de solução:
1 mol de NaOH ------------------ 342 g
X ------------------ 136,8 g
X = 0,4 mol
2º) Determinar a concentração em mols/L:
0,4 mol de NaOH ------------------- 0,8 L de solução
X ------------------- 1,0 L de solução
X = 0,5 mol de NaOH
Desta forma ficamos com : [NaOH] = 0,5 mol/L
07) Uma solução foi obtida dissolvendo-se 50 g de açúcar
em 950 g de água. Determine a porcentagem em massa e o título desta solução.
Dados:
Massa do soluto = 50 g
Massa do solvente =
950 g
Massa da solução =
1000
g
RESOLUÇÃO
1000 g da solução ------------------ 100%
50 g do soluto ------------------
X
X =
5% de soluto ou Título = 50/1000 = 0,05
PARTES POR MILHÃO (PPM)
Observe a seguinte informação:
A análise química do esgoto descarregado no rio de uma
cidade de tamanho médio mostra que contém 0,0030% de íons fosfato, que é
muito prejudicial aos ecossistemas aquáticos.
Significado: "Há 0,0030 g (ou Kg ou tonelada) de íons
fosfato em cada 100 g (ou kg ou tonelada) de água do rio."
Observe que o valor 0,0030 é muito pequeno, por isso
torna-se mais fácil multiplicar este número por 10.000 e, dessa
forma, obtêm-se a seguinte relação:
"Há 30 g de íons fosfato em cada 1.000.000 g (um milhão de
gramas) de água do rio."
Esta afirmação poderá ser expressa da seguinte forma:
30 ppm (m/m), que significam 30 partes de íons fosfato em
massa por um milhão de partes de água do rio em massa.
Desta forma, podemos afirmar que:
Partes por milhão (ppm) indica a relação de 1 parte do soluto por 1 milhão de
partes do solvente. Para soluções muito diluídas, considerar o volume do
solvente igual ao volume da solução.
Ou ainda:
30 ppm: 30 g de soluto por 1.000.000 g da solução
Equivalem a:
30 g de soluto por 1.000 kg de solução, ou
30 g de soluto por 1 tonelada de solução, ou
30 mg de soluto por 1.000.000 mg de solução, ou
30 mg de soluto por 1.000 g de solução, ou
30 mg de soluto por 1 kg de solução.
Analogamente, teremos:
Porcentagem: referência a um total de 100
(102)
Partes por mil: referência a um total de 1.000 (103)
Partes por milhão: referência a um total de
1.000.000 (106)
Partes por bilhão: referência a um total de
1.000.000.000 (109)

A PETROBRÁS descumpriu a resolução do Conselho Nacional do Meio Ambiente (Conama,
de 2002, que estabelecia que os níveis de enxofre no diesel deveriam ser
reduzidos a partir de janeiro de 2009 para 50 partes por milhão (ppm) –
mesmo padrão europeu. Hoje as regiões metropolitanas recebem o óleo com 500
ppm de enxofre, e o resto do País, com 2 mil ppm de enxofre.


Mercúrio é um metal líquido altamente tóxico a qualquer forma de vida, sendo
utilizado na garimpagem de ouro. Depois de retirado,o cascalho do rio é
misturado ao mercúrio liquido.O ouro em pó do cascalho se aglutina ao
mercúrio e o resto é jogado fora.Aquece-se então a mistura mercúrio/ouro até
que os dois se separam.Durante esse processo, 55% do mercúrio evapora; o
restante acaba sendo jogado nos rios. Para cada quilo de ouro retirado dos
rios brasileiros, usa-se de 1,5 a 3 quilos de mercúrio.No leito dos rios o
mercúrio reage com os sedimentos orgânicos e é consumido pelos peixes.A
outra parte que evaporou acaba se condensando e assumindo sua forma líquida
original.Daí temos a poluição dos rios,terras,vegetação,meio ambiente e,
finalmente, do homem.A tolerância do mercúrio nos seres humanos é de 0,02
ppm(partes por milhão) no sangue e de 0,2 ppm na urina.Na natureza, os
teores de mercúrio são baixos,chegando a 1 ou 2 ppm em certos solos.Alguns
garimpos brasileiros já apresentaram contaminação até 2 mil vezes superior à
tolerância biológica.Em Serra Pelada, no Pará,a amostra do cabelo de um
garimpeiro mostrou uma taxa de 2,92 ppm de mercúrio.Muitos peixes migram
para outros rios para a desova; assim, peixes contaminados pelo mercúrio de
um rio,podem levar essa poluição a outras regiões.O garimpo de ouro muitas
vezes utilizam mercúrio contrabandeado, o que torna a operação ilegal. Muito
ouro extraído sai do Estado de forma ilegal, sem tributação.
RELAÇÃO MASSA/MASSA
Exemplos
1) Solução 20 ppm (m/m)
Significado: 20 g de soluto em 1 milhão de gramas da
solução
Obs.: Como a solução é muito diluída, a massa do solvente
é praticamente a massa da solução.
2) 10 ppm de O2 na água (m/m)
Significado: 10 g de O2 dissolvidos em 1 milhão
de gramas de água, ou ainda, 10 mg de O2 dissolvidos em 1 milhão
de miligramas de água.
Obs.: Como 106 mg = 1 kg, ou ainda, 1 ton = 106 g
Desta forma ficamos com: 10 g de O2 dissolvidos
em 1 ton de água, ou ainda, 10 mg de O2 dissolvidos em 1 kg de
água.
Com isso poderemos representar ppm (m/m) pelas relações
matemáticas:


Exercício resolvido
Como se expressa em ppm a padronização: 5 . 10-4
mg de Hg/grama de água.
Dados:
Massa do soluto = 5 . 10-4 mg
Massa do solvente = Massa da solução = 1 g =
10-3 kg
Resolução
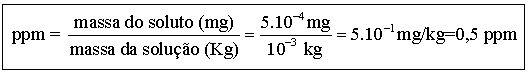
ou ainda...
5 .
10-4
mg de Hg ------------------ 10-3 kg de água (1g)
X ------------------
1 kg (1 ppm)
X =
0,5
mg/kg ou 0,5 ppm
RELAÇÃO MASSA/VOLUME
Como a água possui d = 1 g/mL ou 1 kg/L, logo temos: massa
= volume
desta forma ficamos com: 1g de H2O = 1 mL de H2O,
ou ainda, 1 kg H2O = 1 L de H2O
Exemplos
1) A água imprópria para consumo possui 0,5 ppm em íons Pb2+.
Significado (m/m): 0,05 g de Pb2+ em 106
g de H2O
Como 106 g de H2O = 106
mL, então:
Significado (m/v): 0,05 g de Pb2+ em 106
mL de H2O
Como: 106 mL = 103 L
Então ficamos com:
Significado (m/v): 0,05 g de Pb2+ em 103
L de H2O ou 0,05 mg de Pb2+ em 1 L de H2O.
Com isso poderemos representar ppm (m/v) pelas relações
matemáticas:


Exercício resolvido
Uma xícara de chá preto contém 0,3 mg de flúor. Se o
volume de água na xícara é de 200 mL, qual a concentração em ppm do flúor
nesta solução?
Dados:
Massa do soluto = 0,3 mg
Volume da solução =
200 mL = 0,2 L
Resolução
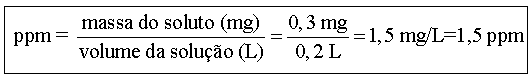
ou ainda...
0,3 mg de Hg ------------------ 0,2 L de
solução
X ------------------
1 L (1 ppm)
X =
1,5
mg/L ou 1,5 ppm
RELAÇÃO VOLUME/VOLUME
Exemplo
Ar considerado bom deve ter concentração de CO no máximo
4,5 ppm ao longo de 8 horas.
Significado 4,5 ppm (v/v): 4,5 L de CO em 106 L
de ar, ou ainda, 4,5 mL de CO em 106 mL de ar
Como: 106 mL = 103 L = 1 m3,
logo ficamos com:
4,5 mL de CO em 1 m3 de ar.
Com isso poderemos representar ppm (v/v) pela seguinte relação
matemática:

Existem duas formas de
concentração de menor importância apresentamos a seguir:
1. Fração Molar do Soluto (x1)
e do Solvente (X2)
A fração do soluto (x1),
em uma solução, é a relação entre a quantidade em mols do soluto (n1)
e a quantidade total em mols das substâncias que constituem a solução (n).
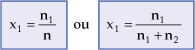
Onde:
n1
= quantidade em mols do soluto
n2
= quantidade em mols do solvente
n = quantidade em mols da solução
Analogamente, para a fração molar
do solvente, pode-se escrever:
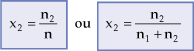
x1
e x2 não possuem
unidade.
Observação
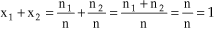 →
→
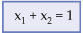
Exemplo:
A 40 g de NaOH, adicionou-se 900 g
de água. Qual a fração molar do soluto e a do solvente, nesta solução?
dados:
NaOH = 40 g/mol
H2O
= 18 g/mol
(1) NaOH
(2) H2O
m1
= 40 g
M1
= 40 g/mol
M2
= 18 g/mol
x1
= ?
x2
= ?
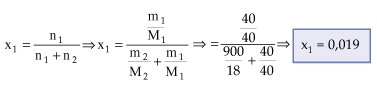
Como x1
+ x2 = 1, x2
= 1 - 0,019 →
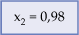
2. Molalidade (W)
Indica a quantidade em mols de
soluto presente em 1 kg de solvente.
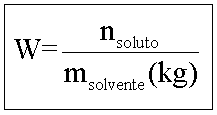
Exemplo
Preparou-se uma solução
dissolvendo 80 g de NaOH em 500 g de água. Qual a molalidade da referida
solução?
Dados: Na = 23; O = 16; H = 1
Soluto (1) NaOH
Solvete (2) H2O
m1
= 80 g
M1
= 40 g/mol
m2
= 500 g = 0,5 kg
W = ?
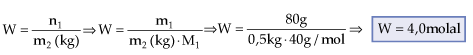
DILUIÇÃO
Diluir uma solução consiste
em adicionar uma quantidade de solvente puro, que provoca uma mudança no
volume, mudando com isso a proporção soluto/solvente e, portanto, a
concentração da solução se altera (diminui).
Consideremos o seguinte sistema:
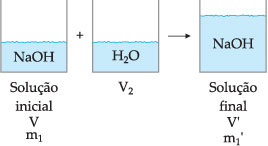
Para a solução inicial:
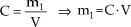
Para a solução final:
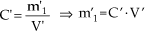
Como foi adicionado apenas
solvente, não alteramos a quantidade de soluto (m1 = m'),
portanto:
C · V = C’ · V’
Utilizando o título, encontramos:
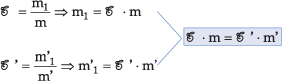
Utilizando a concentração molar:

Não esquecendo que
V’ = V + V2
ou m’ = m + m2
Observação
Concentrar uma solução significa
aumentar a concentração pela retirada de solvente. O solvente é retirado por
meio de uma evaporação, desde que o soluto não seja volátil. As fórmulas
utilizadas são as mesmas apresentadas anteriormente, apenas, ao invés de
aumentar o volume final, ele deve diminuir.
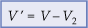
Exercício resolvido
Quanto de água deve ser acrescentado à 100 mL de álcool
96%(v) a fim de transformá-lo 46%(v).
Resolução
1ª Opção (Utilizando a fórmula)
% . V = %' . V'
→ 96 . 100 = 46 . V'
→
V' = 208,7 mL
Vágua =
V' - V = 208,7 mL - 100 mL →
Vágua = 108,7 mL
2ª Opção (Interpretação
por regra de três)
Antes da diluição:
Vsolução = 100
mL
%soluto =
96% (v) →
96 mL
Após a diluição
%soluto =
46% (v) →
46 mL
Vsolução = ?
100
mL de solução →
96 mL de soluto
X
→
46 mL de soluto
X = 208,7 mL de solução
Cálculo do volume de água
acrescentado:
Vágua = Vapós
a diluição - Vantes da diluição
→
Vágua = 208,7 - 100 = 108,7 mL
Mistura de Soluções de Mesmo Soluto
Consideremos o esquema abaixo:
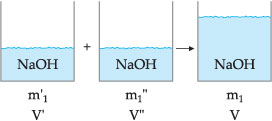

Utilizando o título, o raciocínio é o
mesmo, portanto:

Exercício resolvido
Calcule a concentração (g/L) de um detergente proveniente
da mistura de 300 mL de detergente 30 g/L com 200 mL de detergente 50 g/L.
Resolução
1ª Opção (Utilizando a fórmula)
C
. V = C' . V' + C" . V" →
C . 0,5 = 30 . 0,3 + 50 . 0,2 →
C . 0,5 = 9 + 10
→ C = 38 g/L
2ª Opção (Interpretação
por regra de três)
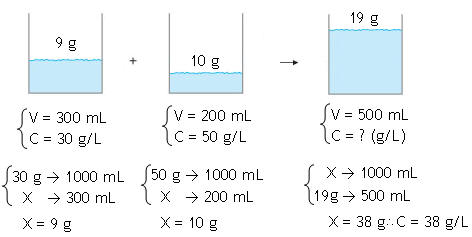
Misturas de Soluções com Reação Química
Neste caso, os exercícios são
resolvidos como na estequiometria, ou seja:
a) montar a equação química:
b) balancear a equação química;
c) determinar a quantidade em mols
de cada reagente;
d) fazer a proporção em mols.
Exemplo
Misturam-se para reagir 1,0 L de
solução 2,0 M de NaOH, com 0,5 L de solução 4,0 M de HCl.
a) A solução final, após a
mistura, será ácida, básica ou neutra?
b) Calcule a concentração molar da
solução final em relação ao sal formado.
Esquematicamente, temos:
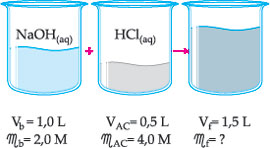
Resolução
1o
passo: montar a equação envolvida na mistura,
balanceá-la e relacionar os coeficientes com quantidades em mols de
reagentes e produtos.
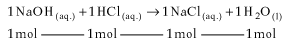
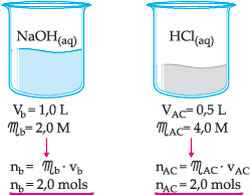
2o
passo: determinar a quantidade em mols de cada
soluto nas soluções a serem misturadas.
3o
passo: verificar se a quantidade de cada reagente
(em mols) está na proporção indicada pela equação do problema.
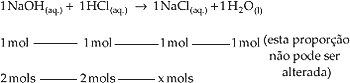
Como as quantidades do NaOH e do
HCl estão na proporção correta, todo ácido e toda base irão reagir (não
haverá excesso), produzindo 2 mols de NaCl, que estarão dissolvidos em 1,5 L
de solução (volume da solução final).
Respostas
a) A solução final será neutra.
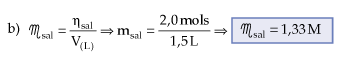
Titulação

Consiste em determinar a concentração de uma solução, pela
reação com outra solução de concentração conhecida. Podemos dizer que a
titulação é a principal operação da chamada análise volumétrica ou
volumetria realizada em laboratório, onde a solução padrão (concentração
conhecida) contida em uma bureta é misturada gota a gota na solução problema
(concentração desconhecida) existente em um erlenmeyer. A solução problema
deve apresentar algumas gotas de indicador para determinar o final da
titulação, em virtude da mudança de cor da mesma.
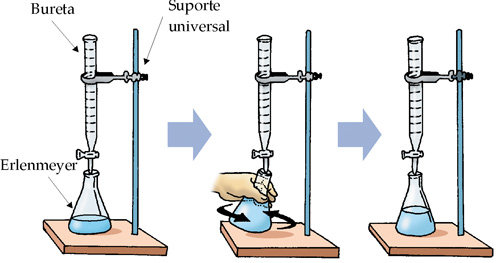
O ponto final da titulação é conhecido como ponto de
viragem. Como a titulação consiste de uma reação entre o soluto da solução
padrão e o soluto do problema, os problemas devem ser resolvidos por
estequiometria.
Exemplo
Retiramos, com auxílio de uma pipeta, 50 mL da solução
contida no frasco abaixo, (observe que a solução possui concentração molar
desconhecida) e transferimos para um frasco erlenmeyer.
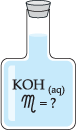
No frasco erlenmeyer, contendo a solução básica,
adicionamos algumas gotas de fenolftaleína, um indicador que, na presença de
base, adquire a coloração avermelhada.
Com o auxílio de uma bureta (figura a seguir), adicionamos
cautelosamente à solução contida no erlenmeyer uma solução de HCl(aq)
2,0 M.
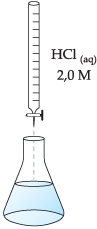
Assim, no erlenmeyer haverá a seguinte reação,
representada pela equação.
1 HCl(aq)
+ 1 KOH(aq)
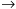 1 KCl(aq) + 1 H2O(l)
1 KCl(aq) + 1 H2O(l)
Pela equação, observaremos que a neutralização entre o
ácido e a base será completa quando o número de mols de
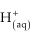 do ácido for igual ao número de mols de
do ácido for igual ao número de mols de
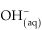 da base.
da base.
Esse fato é verificado exatamente no momento em que a
coloração vermelha, devido ao meio básico, muda para incolor. Neste momento,
o número de mols
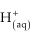 ,
provenientes do ácido neutralizam totalmente o número de mols do
,
provenientes do ácido neutralizam totalmente o número de mols do
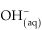 ,
provenientes da base.
,
provenientes da base.
Anotamos o volume de ácido gasto (25 mL), e calculamos
quantos mols do ácido foram utilizados para reagir completamente com a base.
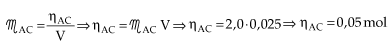
Vejamos agora como se calcula a
concentração molar do KOH(aq):
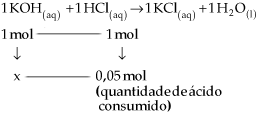
x = quantidade em mols de OH–
presente no erlenmeyer = 0,05 mol
Assim, para calcular a
concentração molar da base:
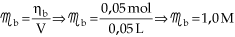
Exercício resolvido
Por lei, o vinagre (solução aquosa de ácido acético) pode
conter, no máximo 4% em massa (0,67 mol/L) de ácido acético. Para você
verificar se o vinagre utilizado em sua casa atende às especificações
legais, para isso você verifica que 40 mL de vinagre são neutralizados por 8
mL de solução aquosa de NaOH 2 M. A que conclusão você chegou?
Dados:
Vinagre: V = 40 mL = 0,04 L, [ác. acético] =
? (mols/L)
NaOH(aq): V = 8 mL = 0,008 L, [NaOH] = 2
mols/L
RESOLUÇÃO
Cálculo do número de mols de NaOH que
reage:
2 mols de NaOH
→ 1 L de solução
X
→
0,008 L de solução
X = 0,016 mol
Cálculo do número de mols
de ác. acético que será neutralizado pelo NaOH:
CH3-COOH
+ NaOH →
CH3-COO-Na+ + H2O
1 mol
1 mol
X
0,016 mol
X = 0,016 mol
Cálculo da [ác. acético]
no vinagre:
0,016 mol de ác.
acético →
40 mL de vinagre
X
→ 1000
mL de vinagre (1 L)
X = 0,4 mol, com isso temos que: [ác. acético] = 0,4 mol/L
Como a concentração de ác.
acético máxima exigida por lei, no vinagre, é de 0,67 mol/L, com isso
concluímos que a amostra de vinagre analisada não atende às especificações
exigidas.
Home | Soluções | Cinética Química | Termoquímica | Oxirredução | Eletroquímica | Equilíbrio Químico | Propriedades Coligativas
Este site foi atualizado em
04/03/19



 A
receita que acompanha a embalagem de uma gelatina em pó descreve
o seguinte método de preparação:
A
receita que acompanha a embalagem de uma gelatina em pó descreve
o seguinte método de preparação: A
proteína mais abundante dos vertebrados é o colágeno, que
constitui aproximadamente 25% em massa das proteínas do corpo
humano. Parte dos ossos, tendões, dentes e pele é constituída de
colágeno.
A
proteína mais abundante dos vertebrados é o colágeno, que
constitui aproximadamente 25% em massa das proteínas do corpo
humano. Parte dos ossos, tendões, dentes e pele é constituída de
colágeno. Você
provavelmente se lembra de que os orgânulos do citoplasma estão
mergulhados num material amorfo, viscoso, chamado hialoplasma.
Como componente majoritário, o hialoplasma contém, antes de mais
nada, muita água. Em segundo lugar, em termos de quantidade,
encontramos moléculas de proteínas.
Você
provavelmente se lembra de que os orgânulos do citoplasma estão
mergulhados num material amorfo, viscoso, chamado hialoplasma.
Como componente majoritário, o hialoplasma contém, antes de mais
nada, muita água. Em segundo lugar, em termos de quantidade,
encontramos moléculas de proteínas.  Todos
sabemos que água e óleo não se misturam e isso habitualmente é
justificado pelo fato da água ser um líquido polar, enquanto o
óleo é formado por moléculas praticamente apolares.
Todos
sabemos que água e óleo não se misturam e isso habitualmente é
justificado pelo fato da água ser um líquido polar, enquanto o
óleo é formado por moléculas praticamente apolares. Para
fazer maionese, basta colocar uma gema do ovo em um
liquidificador, bater vigorosamente e acrescentar um pouco de
óleo. Forma-se, assim, uma emulsão estável.
Para
fazer maionese, basta colocar uma gema do ovo em um
liquidificador, bater vigorosamente e acrescentar um pouco de
óleo. Forma-se, assim, uma emulsão estável. A
figura ao lado representa esquematicamente a estrutura de um
tensoativo. Eles reduzem a tensão superficial da água,
permitindo que a sujeira possa ser removida facilmente ou mesmo
que um óleo possa se misturar com a água, através da formação de
micelas.
A
figura ao lado representa esquematicamente a estrutura de um
tensoativo. Eles reduzem a tensão superficial da água,
permitindo que a sujeira possa ser removida facilmente ou mesmo
que um óleo possa se misturar com a água, através da formação de
micelas. remoção das sujidades, que envolve o deslocamento das partículas
de sujeiras de natureza lipofílica para o interior das micelas e
a estabilização das mesmas de modo a mantê-las em suspensão,
evitando que a sujeira volte a depositar-se sobre a superfície
que está sendo limpa.
remoção das sujidades, que envolve o deslocamento das partículas
de sujeiras de natureza lipofílica para o interior das micelas e
a estabilização das mesmas de modo a mantê-las em suspensão,
evitando que a sujeira volte a depositar-se sobre a superfície
que está sendo limpa.

 Neblinas , fumaças e
sprays são outros exemplos de aerossóis do cotidiano. Quando
observamos o rastro luminoso deixado pela luz de um projetor de
slides em uma sala escura, ou quando notamos os feixes luminosos
dos faróis dos carros em dias com forte neblina, devemos nos
lembrar do efeito Tyndall que a luz pode provocar quando atinge
partículas coloidais sólidas existentes no ar.
Neblinas , fumaças e
sprays são outros exemplos de aerossóis do cotidiano. Quando
observamos o rastro luminoso deixado pela luz de um projetor de
slides em uma sala escura, ou quando notamos os feixes luminosos
dos faróis dos carros em dias com forte neblina, devemos nos
lembrar do efeito Tyndall que a luz pode provocar quando atinge
partículas coloidais sólidas existentes no ar.









 Todo
aumento de temperatura diminui a solubilidade do gás no líquido – Por
exemplo, para eliminar gases dissolvidos na água, é feito o aquecimento por
um certo período de tempo. Sendo assim, a diminuição da temperatura facilita
a solubilidade de um gás num líquido - Por exemplo, na piracema os peixes
nadam contra a corrente para realizar a desova nas nascentes onde as águas
são mais oxigenadas, portanto, facilitando a reprodução e desova.
Todo
aumento de temperatura diminui a solubilidade do gás no líquido – Por
exemplo, para eliminar gases dissolvidos na água, é feito o aquecimento por
um certo período de tempo. Sendo assim, a diminuição da temperatura facilita
a solubilidade de um gás num líquido - Por exemplo, na piracema os peixes
nadam contra a corrente para realizar a desova nas nascentes onde as águas
são mais oxigenadas, portanto, facilitando a reprodução e desova.