O Átomo Nuclear
No final do século XIX, o elétron já estava estabelecido
como partícula fundamental, principalmente depois de 1897, ano
em que J. J. Thomson determinou a sua razão carga/massa.
E já se sabia que elétrons eram liberados por emissão
termoiônica (de um metal a alta temperatura), no efeito
fotoelétrico e no decaimento
b de certos elementos
radioativos.
Desse modo, os elétrons já eram considerados como
constituintes básicos dos átomos.
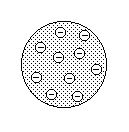
Segundo o modelo atômico apresentado em 1904 por J. J.
Thomson, o átomo deveria ser constituído por algum tipo de
fluido de forma esférica, com uma distribuição contínua de carga
positiva, e de elétrons com carga negativa distribuídos no
fluido em número suficiente para que a carga total do sistema
fosse nula.
O modelo exigia dos elétrons que tivessem movimentos
oscilatórios ao redor de certas posições que definiriam
configurações estáveis para o sistema.
E como, segundo a teoria eletromagnética clássica, qualquer
partícula com carga elétrica em movimento acelerado emite
radiação eletromagnética, o modelo também exigia que os modos
normais das oscilações dos elétrons tivessem as mesmas
freqüências que aquelas observadas associadas às raias dos
espectros atômicos.
Contudo, segundo a teoria eletromagnética clássica, não
pode existir qualquer configuração estável num sistema de
partículas carregadas se a única interação entre elas é de
caráter eletromagnético.
Além disso, não foi encontrada qualquer configuração para
os elétrons de qualquer átomo cujos modos normais tivessem
qualquer uma das freqüências esperadas.
De qualquer modo, o modelo de Thomson foi abandonado
principalmente devido aos resultados do experimento de
Rutherford.
Experimento de Rutherford
Na época em que J. J. Thomson propôs seu modelo, H. Geiger
e E. Marsden estudavam o espalhamento de feixes bem colimados de
partículas
a,
que já se sabia serem núcleos de átomos de hélio, por finas
folhas de ouro, pelo que hoje se conhece como o experimento de
Rutherford.
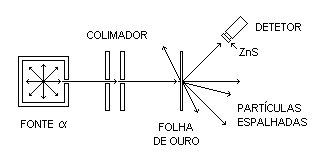
Uma fonte radioativa emite partículas
a
que são colimadas, formando um feixe paralelo e estreito, que
incide sobre uma folha metálica muito pouco espessa. Para que
fosse possível construir tal folha, a maleabilidade do metal
deveria ser grande e, por isso, era usado normalmente o ouro.
A folha é tão fina que as partículas a atravessam
completamente com apenas uma pequena diminuição no módulo da
velocidade. Ao atravessar a folha, entretanto, cada partícula
a
sofre muitos desvios devido a sua interação eletrostática com as
cargas positivas e negativas dos átomos da folha.
As partículas espalhadas eram detectadas por um microscópio
com uma tela de sulfeto de zinco (ZnS).
A tela de sulfeto de zinco cintila no local onde incide uma
partícula
a.
O microscópio permite identificar a cintilação de cada partícula
a
individualmente.
Os resultados experimentais de Geiger e Marsden mostraram
que o número de partículas a
que eram desviadas com ângulos maiores do que 90 graus era muito
maior que o esperado pelo modelo de Thomson.
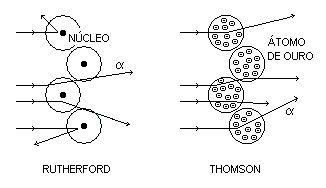
Em 1911, E. Rutherford mostrou que os dados de Geiger e
Marsden eram consistentes com um modelo atômico em que a carga
positiva do átomo se concentrava em uma pequena região que, além
disso, continha praticamente toda a massa do átomo, com os
elétrons espalhados ao redor dessa pequena região (chamada
núcleo).
O raio de um núcleo típico é cerca de dez mil vezes menor
que o raio do átomo ao qual pertence mas contém mais de 99,9% da
massa desse átomo.
Física Nuclear