





|
|
|
|
 |

|
|
 Tudo
começou com um grande erro.
Em 1855, a Sociedade Farmacêutica de Paris ofereceu um
prêmio para o primeiro cientista capaz de isolar o princípio
ativo da Cannabis sativa. O contemplado foi J. Personee
(J. Pharm. Chim. 1855, 28, 461–463),
um químico francês. Nem um mês se passou para que a
comunidade científica da época constatasse o equívoco:
o óleo extraído por Personee
não era ativo! Não continha nenhum componente com
atividade fisiológica - ao contrário da cannabis. Foi
Vignolo, um químico italiano, que descobriu o erro: o óleo
de Personee era rico em sesquiterpenos, substâncias
abundantes na cannabis, mas sem atividade biológica. Durante
várias décadas, a busca pelo princípio ativo da cannabis
continuou, em todo o mundo. Enquanto que a morfina, a
cocaína, a strychnina, a cafeína e outros alcalóides
eram isolados e caracterizados, nenhuma novidade aconteceu
com a cannabis. Isto porque, ao contrário dos alcalóides -
que são facilmente isolados na forma de sais - os
terpenóides (tal como o THC) requerem técnicas químicas mais
apuradas, inexistentes até 80 anos atrás. O primeiro químico
a obter um extrato ativo da cannabis foi Wood, em
1896, na Cambridge University (J. Chem.
Soc. 1899, 75, 20-36). Segundo palavras do
próprio autor: "The red oil,
is extremely active, and taken in doses of 0.05 g induces
decided intoxication followed by sleep. The symptoms
produced by it are peculiar to Cannabis indica, and as none
of the other products appear to possess this action, this
substance must be regarded as the active constituent of the
plant." Tudo
começou com um grande erro.
Em 1855, a Sociedade Farmacêutica de Paris ofereceu um
prêmio para o primeiro cientista capaz de isolar o princípio
ativo da Cannabis sativa. O contemplado foi J. Personee
(J. Pharm. Chim. 1855, 28, 461–463),
um químico francês. Nem um mês se passou para que a
comunidade científica da época constatasse o equívoco:
o óleo extraído por Personee
não era ativo! Não continha nenhum componente com
atividade fisiológica - ao contrário da cannabis. Foi
Vignolo, um químico italiano, que descobriu o erro: o óleo
de Personee era rico em sesquiterpenos, substâncias
abundantes na cannabis, mas sem atividade biológica. Durante
várias décadas, a busca pelo princípio ativo da cannabis
continuou, em todo o mundo. Enquanto que a morfina, a
cocaína, a strychnina, a cafeína e outros alcalóides
eram isolados e caracterizados, nenhuma novidade aconteceu
com a cannabis. Isto porque, ao contrário dos alcalóides -
que são facilmente isolados na forma de sais - os
terpenóides (tal como o THC) requerem técnicas químicas mais
apuradas, inexistentes até 80 anos atrás. O primeiro químico
a obter um extrato ativo da cannabis foi Wood, em
1896, na Cambridge University (J. Chem.
Soc. 1899, 75, 20-36). Segundo palavras do
próprio autor: "The red oil,
is extremely active, and taken in doses of 0.05 g induces
decided intoxication followed by sleep. The symptoms
produced by it are peculiar to Cannabis indica, and as none
of the other products appear to possess this action, this
substance must be regarded as the active constituent of the
plant."
A história do THC na
química é ainda mais bizarra: tivemos
conhecimento da versão sintética antes de isolarmos a versão
natural! Em 1930, Cahn isolou o cannabinol - extraído a
partir do óleo de Wood. Na época, acreditava-se que o
cannabinol fosse o principal ingrediente ativo da cannabis.
O químico americano Adams e o britânico Todd, na década de
1940, desenvolveram várias rotas sintéticas para análogos do
cannabinol. Para sua surpresa, uma das rotas levou a um
composto com intensa atividade biológica, muito maior do que
o cannabinol. Era o d-9-THC (J.
Amer. Chem. Soc. 1949, 71, 1624-1628).
Dentre os vários derivados preparados, o
d-9-THC era o mais ativo. Os
químicos da época, então, desconfiaram que a cannabis
deveria ter, também, este terpenóide. Entretanto, foi
somente em 1964 que a primeira isolação do
d-9-THC na forma pura ocorreu. Os
químicos Gaoni and Mechoulam obtiveram, de uma extração com
hexano de uma amostra de hashish, vários cannabinóides,
entre ele o d-9-THC,
na forma cristalina.
Maior até do que dos
usuários, o interesse dos cientistas pela
marijuana está sempre se renovando:
todos ficam fascinados pelo poder que as substâncias
contidas nesta planta exercem sobre o homem. Entretanto, foi
somente em 1988 que a pesquisa sobre a maconha deu um grande
salto: Howlett et al. (Mol.
Pharmacol. 33, 297-302) descobriram a existência
de neurorecpetores para os compostos cannabinóides: isto é,
determinados grupos de proteínas existentes em alguns
neurônios cujo objetivo era unicamente o de se ligar a
compostos com estrutura química semelhante a dos
cannabinóides. Howlett chamou estes receptores de
CB1; em 1993, outro grupo de receptores para cannabinóides
foi descoberto, desta vez por Munro et at. (Nature
1993;365:61). Munro chamou este novo grupo
de receptores como CB2.
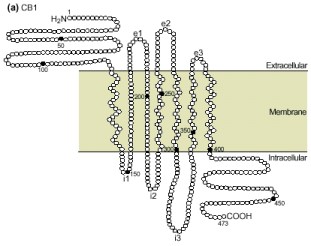
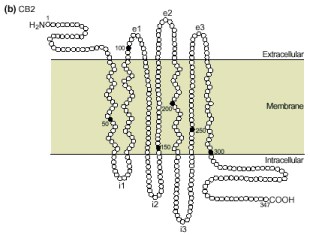
Receptores cannabinóides CB1 e CB2, sequenciados
pelo GenBank. Ambos receptores são polipeptídeos com
sete a-hélices transmenbrana e possuem N-terminais
extracelulares glicosilados e C-terminais
intracelulares. O receptor CB1 é maior do que o
receptor CB2, nas regiões intra e extra celular. Na
região transmembrana os dois receptores tem 78% de
similaridade.
|
Diversas pesquisas, desde então, mostraram que
os efeitos farmacológicos da
marijuana são mediados por estes dois receptores.
Ambos ativam mecanismos de transdução similares, incluindo a
inibição da adenilate ciclase e de canais de Ca2+
do tipo N. O CB1 ocorre no cérebro, onde é responsável por
efeitos característicos da cannabis (relaxação, bem-estar,
analgesia, aumento da percepção audio-visual, depressão da
atividade motora, analgesia e catalapsia) e também no
sistema nervoso periférico. Aí, os receptores CB1 são
localizados pressinapticamente e sua ativação pode produzir
uma supressão da liberação de neurotransmitores. Os
principais sintomas da ativação destes receptores são a
estimulação do apetite, vasodilatação (particularmente dos
vasos conjuntivos), taquicardia e inibição da mobilidade
instestinal.
Os receptores CB2, até agora, somente foram localizados fora
do SNC (sistema nervoso central), principalmente em células
do sistema imunológico. Muitos autores relacionam a ativação
destes receptores com imunosupressão, efeitos
anti-inflamatórios e analgesia associada a processos
inflamatórios. Ao contrário dos receptores CB1, pouco se
sabe, ainda, sobre este grupo de receptores.
Era quase inconcebível
para a maior parte dos neurologistas que o
cérebro animal fosse gastar parte de seus nutrientes e
mecanismos simplesmente para elaborar um receptor para uma
substância provinda de uma planta. Tal como com a morfina, a
descoberta de receptores biológicos para cannabinóides
exógenos levantou a possibilidade para a
existência de cannabinóides
endógenos. Muitos químicos e bioquímicos, então,
focaram seus esforço no sentido de descobrir candidatos a
ocupar esta posição: cannabinóides endógenos.
|
QMCWEB://
Tema.de.Casa
|
Chemistry and
Physics of Lipids 108 (2000) 1–13
 O esquema acima
representa uma das rotas sintéticas para o THC.
Identifique os tipos de reações envolvidas em
cada passo e os reagentes necessários para as
mesmas. Submeta sua resposta para:
O esquema acima
representa uma das rotas sintéticas para o THC.
Identifique os tipos de reações envolvidas em
cada passo e os reagentes necessários para as
mesmas. Submeta sua resposta para:
temadecasa@qmcweb.org
|
O primeiro ligante cannabinóide
endógeno a ser isolado foi a etanolamida da arachidonila,
chamada de anandamida.
O nome vem da palavra "ananda", cujo significa em
sânscrito é "prazer". Tão logo esta descoberta foi
anunciada, centenas de veículos de comunicação publicaram
manchetes como "Descoberta a molécula do prazer", ou
"Cérebro produz maconha". Obviamente, um péssimo jornalismo
científico, como sempre. Na verdade, a anandamida tem poucos
efeitos similares ao THC, além de ser facilmente hidrolisada
quando em contato com o receptor. Porém, várias situações
estimulam o organismo a despejar grandes quantidades de
anandamida nas fendas sinápticas: autores sugerem que esta
droga esteja relacionada a momentos de relaxamento, prazer e
calma. Um derivado sintético da anandamida - a metanandamida
- possui uma potência mais elevada e maior estabilidade e
mostrou-se portadora de grande efeito fisiológico. Outros
derivados eicosanóides capazes de se ligarem aos receptores
cannabinóides já foram isolados dos mais distintos tecidos
humanos. Entre estes, o 2-arachidoniglicerol,
considerado um dos mais potentes cannabinóides endógenos.
Cientistas estavam intrigado com o fato de que muitas
pessoas deprimidas recorriam ao consumo de chocolate nos
picos depressivos. Foi somente em 1996 (Nature
1996;382:677), que Di Tomaso e colaboradores
indentificaram no pó de cacau e no
chocolate
um grupo de substâncias capazes de interagir
com os receptores
cannabinóides. Entre estas substâncias, estavam a
anandamida (ela mesma!) e também dois compostos que podem
interferir na hidrólise biológica da anandamida, a
N-oleoiletanolamina e N-linoleoiletanolamina.
Estes estimuladores cannabinóides, em conjunto com outros
ingredientes ativos do chocolate (metilxantinas e aminas
biogênicas) talvez justifiquem a fabulosa atração que
estes doces exercem sobre as pessoas.
|
Tão logo se fez a descoberta dos receptores cannabinóides e
dos cannabinóides endógenos, cientistas do mundo todo
passaram a brincar de química orgânica e sintetizar os mais
variados agonistas e antagonistas cannabinóides possíveis,
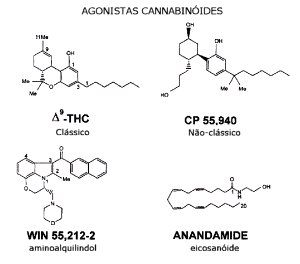
para estudar as suas atividades biológicas. Embora o número
seja imenso, os agonistas
cannabinóides (incluindo os sintéticos) podem ser
separados em 4 grandes grupos:
não-clássicos, clássicos,
aminoalquilindols e eicosanóides. O grupo
clássico são os derivados do dibenzopirano - tal como o THC.
O grupo não-clássico consiste em substâncias bicíclicas ou
tricíclicas, similares ao THC, mas sem o anel pirano. O mais
comum é o agonista sintético CP55940. Os demais grupos têm
estruturas bastante distintas da do THC.
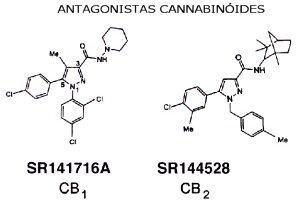
Os cannabinóides
antagonistas exercem um efeito completamente
oposto nos receptores CB1 e CB2 do que o dos agonistas. O
composto SR141716A (patenteado pela empresa francesa
Sanofi Recherche), por exemplo, é um dos
antagonistas mais estudados. Seus efeitos, em ratos, incluem
a supressão do apetite, o incremento da mobilidade
intestinal, a melhora da memória recente e aumenta a
liberação de neurotransmissores por neurônios centrais e
periféricos.
Enquanto o debate sobre a liberação da maconha para uso
medicinal continua, vários
cannabinóides sintéticos já
estão sendo utilizados pela indústria farmacêutica
ou estão prestes a entrar no mercado. A tabela abaixo mostra
algumas aplicações terapêuticas para agonistas e
antagonistas do sistema cannabinóide endógeno.
|
Uso terapêutico para drogas cannabinóides
|
|
Drogas |
Uso |
|
agonistas do CB1 |
Tratamento do câncer
Dor pós cirúrgica
anticonvulsivo
Antispástico em escleroses múltiplas |
|
agonistas do CB1 periférico |
Incrementador do apetite
Disfunções glandulares |
|
agonistas do CB2 |
Dor inflamatória periférica
Immunosupressão |
|
antagonistas do CB1 |
Deficiência de memória
Tratamento da obesidade
Dependência alcóolica |
|
antagonistas do CB1 periférico |
Disfunções glandulares |
Desde a sua descoberta, os endocannabinóides e os
exocannabinóides têm sido foco de centenas de trabalhos de
química e bioquímica. Os receptores CB1 e CB2 já são
considerados alvos para muitas terapias farmacêuticas. E é
este, agora, o campo de ação para os pesquisadores e
cientistas que trabalham com temas relacionados à cannabis.
Isto prova que, de fato (como proclamam aos quatro ventos os
defensores da liberação da marijuana)
a natureza nos deu a maconha
com um objetivo: o de nos tornar cientes da
existência dos receptores cannabinóides em nossos próprios
organismos!
|
Deu no Jornal!
|
Drug and Alcohol Dependence 63 (2001) 107–116
Ratos "chapados"!
Um grupo de farmacologistas da Virginia Commonwealth
University realizou um interessante trabalho com
ratos, maconha e THC. Os ratos foram submetidos a
inalações de cigarros de maconha (com ou sem THC) e
também a ingeções de THC, e vários padrões de
comportamento, como mobilidade, catalepsia,
antinonicepção foram medidas.
Dentre os resultados, destacam-se a comprovada
analgesia conferida pelo THC: tanto através da
maconha como pelas injeções, os ratos que usaram THC
levavam mais tempo para responder a um estímulo
doloroso.
Em todos os experimentos, um grupo de ratos recebeu,
também, a aplicação do antagonista cannabinóide
SR141416A, que bloqueia a ação do THC.
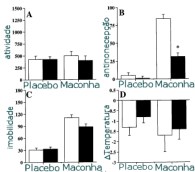
Resultados com inalação da
fumaça de marijuana. No placebo, a marijuana havia
sido extraída com etanol para a retirada dos
cannabinóides. (as barras cheias refletem
experimentos com administração do antagonista)
Os ratos eram colocados sobre uma plataforma que era
lentamente aquecida. A intensidade do calor era
automaticamente aumentada até se observar uma reação
do rato.
Outra observação interessante era o grau de
imobilidade dos ratos em função da droga; postos em
uma gaiola cheia de fotodiodos que acusavam a
passagem do rato. O número de vezes que o rato
passava pelos feixes luminosos era registrado. E,
finalmente, a temperatura retal dos ratos era medida
antes e depois da administração da droga, sendo
expressa sob a forma de variação de temperatura.
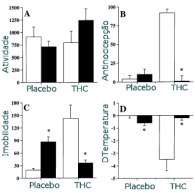
Resultados com administração de injeções de THC. O
placebo continha apenas o veículo. (as barras cheias
refletem experimentos com administração do
antagonista)
Os efeitos da administração do THC via injeção são
muito mais pronunciados do que na inalação da fumaça
da marijuana. Na injeção, também, os efeitos do
antagonista são mais facilmente percebidos.
Entretanto, em ambas as situações a resistência ao
estímulo doloroso é aumentada com o uso da droga
(THC ou marijuana). A imobilidade, também, é maior,
independente da forma de aplicação. A variação da
temperatura retal, porém, só é diferente no caso a
injeção de THC.
Os autores concluem dizendo que a inalação de
marijuana produz efeitos similares ao da
administração de THC e que o efeito medido através
do antagonista indica um mecanismo de absorção da
droga via receptor CB1.

|
|
Deu no Jornal!
|
Journal of Chromatography B, 733 (1999) 119–126
Achando maconha na urina,
saliva, sangue e cabelo!
Você até pode esconder de sua mãe o seu hábito de
fumar maconha. Mas sua mentira não faria sentido
para um químico. Desde 1980, métodos analíticos
foram desenvolvidos para a determinação -
qualitativa e quantitativa - de cannabinóides em
várias matrizes biológicas, como a saliva, o sangue,
o cabelo e a urina.
Dentre as substâncias analisadas, destacam-se - além
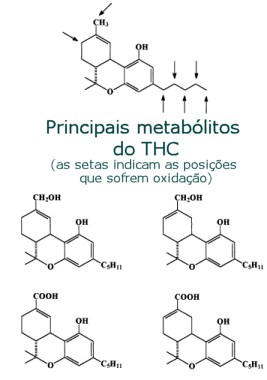
do próprio THC - mais dois cannabinóides e os dois
principais metabólitos, tal como ilustrado nas
estruturas abaixo.
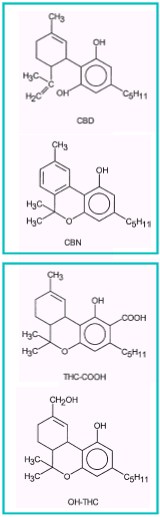
No sangue, as substâncias mais abundantes são o THC
e THC-COOH. A legislação norte-americana proibe a
direção de veículos sob o efeito de drogas. O único
exame aceito, até agora, é o de sangue. Neste caso,
a análise do sangue é interpretada em função de
modelos matemáticos que, de acordo com a relação
entre a concentração do THC e de seus metabólitos no
plasma, são capazes de estabelecer o momento da
exposição do usuário à droga.
No cabelo, THC é a espécie mais abundante e THC-COOH
é detectável apenas em baixas concentrações. Isto
não é surpresa, uma vez que os fatores que
determinam a incorporação de drogas no cabelo são a
liofilicidade, a afinidade por melanina e
permeabilidade na membrana celular. O THC-COOH,
portanto, é menos incorporado que drogas básicas,
pois a permeabilidade na membrana é baseada no
gradiente de pH entre o sangue (pH=7,4) e a matriz
capilar (pH=5).
Comparados com outras matrizes biológicas, os
cannabinóides CBN e CBD são encontrados em
quantidades relativamente altas no cabelo.
É possível se encontrar THC em cabelos de usuários
que já estão em até 12 anos de abstinência!
A determinação de cannabinóides na saliva ainda é um
ponto polêmico e controverso. A presença de THC na
saliva poderia ser atribuida à contaminação da
cavidade oral durante o consumo do baseado. Alguns
autores já foram capazes de detectar concentrações
baixíssimas de cannabinóides na saliva, mas nenhum
trabalho registrou a presença de metabólitos. De
qualquer forma, o teste só é positivo se o consumo
tiver ocorrido pouco tempo antes do teste.
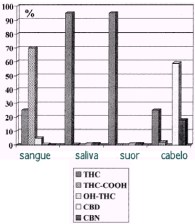
No suor, somente o THC pode ser encontrado e numa
concentração muito baixa. Nenhum trabalho conseguiu
estabelecer um método eficaz para a utilização desta
matriz na detecção de cannabinóides.
Em todos os casos, os métodos para a detecção
envolvem cromatografia gasosa (GC) ou líquida (HPLC),
precedidas de extrações líquido-liquido (LLE) ou
líquido-sólido (SPE) da matriz biológica.
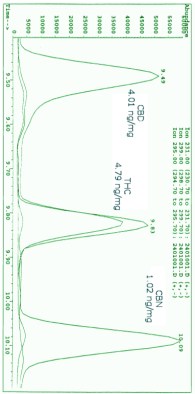
Cromatograma obtido após a
extração de uma amostra de cabelo de um usuário de
maconha.
Muitos métodos desenvolvidos por químicos analíticos
são de uso atual da polícia e perícia técnica, e têm
auxiliado na solução de vários crimes e infrações
ligadas à marijuana.

|
|
 |
|