 TIOCOMPOSTOS
TIOCOMPOSTOS


Tiocompostos são os responsáveis pelo odor característico do alho e do
gambá.
Tiocompostos são obtidos da troca do oxigênio de um
composto por enxofre. Os principais tiocompostos são os
tioálcoois ou tióis,
tioéteres, tiocetonas
e tiofenóis.
Exemplos
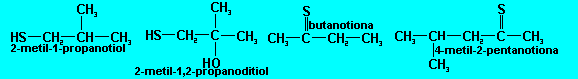
Saiba Mais Sobre Metilmercaptanas...
Existem padrões
oficiais para os níveis aceitáveis de odores desagradáveis, e a
metilmercaptana encabeça esta lista. Esta molécula é a manchete quando é
emitida em grandes quantidades, e algumas vezes isto ocorre porque ela é
usada industrialmente, por exemplo na fabricação de alguns inseticidas e,
compostos similares à metilmercaptana são usados para conferir odor ao gás
natural, facilitando assim a detecção de vazamentos de gás.
A metilmercaptana é também
produzida naturalmente a partir das bactérias presentes no meio ambiente e,
é produzida em nosso organismo quando digerimos a alicina após comer alho ou
tomar uma cápsula de alho.
As bactérias são também as
responsáveis pela formação da metilmercaptana que produzimos em nossas
próprias bocas e que podemos exalar continuamente como mau hálito. A
metilmercaptana pode ser formada a partir de nossas próprias proteínasquando
elas são quebradas pela ação bacteriana. Nós facilmente detectamos a
metilmercaptana quando alguém está conversando conosco - humanos podem
detectá-la no ar em níveis de partes por bilhão -mas, curiosamente, não
temos a capacidade de sentir a metilmercaptana que nós mesmos produzimos.
O mau hálito é causado por várias
moléculas, tais como sulfeto de hidrogênio e sulfeto de dimetila,
 mas o
principal responsável é a metilmercaptana. O sulfeto de hidrogênio, o
tradicional "fedor" dos laboratórios de química, é muito menos cheiroso, o
mesmo sendo válido para o sulfeto de dimetila, que é parte constituinte do
odor do café recém-preparado. Graham Embery, da Universidade de Gales, em
Cardiff, pesquisou as moléculas que contém enxofre e que são encontradas em
nossa boca, provenientes da ação bacteriana. Estas bactérias fragmentam os
aminoácidos cisteína e metionina presentes nas proteínas, originando então a
metilmercaptana. Se o odor de metilmercaptana é muito forte, este é um
indicativo de que a sua gengiva encontra-se doente. A metionina é um
aminoácido essencial para todas as formas de vida, e a proteína animal
contém até 4% deste aminoácido, por isso as bactérias são capazes de liberar
metilmercaptana em quantidade suficiente para tornar o seu hálito
desagradável.
mas o
principal responsável é a metilmercaptana. O sulfeto de hidrogênio, o
tradicional "fedor" dos laboratórios de química, é muito menos cheiroso, o
mesmo sendo válido para o sulfeto de dimetila, que é parte constituinte do
odor do café recém-preparado. Graham Embery, da Universidade de Gales, em
Cardiff, pesquisou as moléculas que contém enxofre e que são encontradas em
nossa boca, provenientes da ação bacteriana. Estas bactérias fragmentam os
aminoácidos cisteína e metionina presentes nas proteínas, originando então a
metilmercaptana. Se o odor de metilmercaptana é muito forte, este é um
indicativo de que a sua gengiva encontra-se doente. A metionina é um
aminoácido essencial para todas as formas de vida, e a proteína animal
contém até 4% deste aminoácido, por isso as bactérias são capazes de liberar
metilmercaptana em quantidade suficiente para tornar o seu hálito
desagradável.
Uma sugestão para aqueles que
exalam quantidades apreciáveis de metilmercaptana é o uso de cremes dentais
que contenham agentes que atuem contra a formação de placas, tais como sais
de zinco e estanho. Estes metais interferem nas enzimas das bactérias que
produzem a metilmercaptana. Tradicionalmente, acredita-se que anti-sépticos
bucais curam o mau hálito, porém eles não fazem mais do que limpar a boca e
disfarçaro odor ofensivo. Uma boa enxaguada com um anti-séptico bucal
eliminará cerca da metade das bactérias bucais. Uma maneira mais popular de
limpar a boca é aumentar a quantidade de saliva, mascando chicletes.
 Nossos
pés podem também conter micróbios que liberam metilmercaptana, especialmente
se fornecemos a eles um ambiente adequado tais como meias sujas e sapatos
abafados. Nos nossos pés as bactérias da classe
Staphylococci e
Coryneform aeróbicos são as
responsáveis pela produção da metilmercaptana. Estas bactérias florescem em
condições de aumento de alcalinidade, condições essas encontradas em meias
sujas e sapatos abafados. Se você tem pés "cheirosos", então a solução
química é colocar em seus sapatos palmilhas especiais contendo carvão - esta
palmilha contém camadas de carbono que absorvem a metilmercaptana. Uma vez
que a quantidade de metilmercaptana é diminuta, as palmilhas funcionarão por
várias semanas.
Nossos
pés podem também conter micróbios que liberam metilmercaptana, especialmente
se fornecemos a eles um ambiente adequado tais como meias sujas e sapatos
abafados. Nos nossos pés as bactérias da classe
Staphylococci e
Coryneform aeróbicos são as
responsáveis pela produção da metilmercaptana. Estas bactérias florescem em
condições de aumento de alcalinidade, condições essas encontradas em meias
sujas e sapatos abafados. Se você tem pés "cheirosos", então a solução
química é colocar em seus sapatos palmilhas especiais contendo carvão - esta
palmilha contém camadas de carbono que absorvem a metilmercaptana. Uma vez
que a quantidade de metilmercaptana é diminuta, as palmilhas funcionarão por
várias semanas.
A metilmercaptana é o membro
mais simples de uma série de compostos nos quais podem existir cadeias de
até 20 átomos de carbono ligados a um átomo de enxofre. A metilmercaptana
apresenta apenas um átomo de carbono. Mercaptanas com três, quatro átomos de
carbono são as que encontramos quando cheiramos o gás de cozinha proveniente
de um vazamento. Uma mercaptana com 18 átomos de carbono em cadeia é usada
como cera em polidores de prata.
 A
maior desvantagem na fabricação e no transporte da metilmercaptana para fins
industriais é o seu baixo ponto de ebulição, de apenas 6°C. Por sorte ela
pode ser facilmente transformada em uma substância química similar, o
dissulfeto de dimetila (DMDS), um líquido amarelo que ferve a 110°C. Este
composto consiste em duas moléculas de metilmercaptana unidas entre si pelos
átomos de enxofre. O DMDS é ligeiramente menos odorífico que a
metilmercaptana, mas é muito mais fácil e seguro de transportar, sendo a
maior parte deste produto produzido na cidade de Lacq, situada no sudoeste
da França, onde o gás natural contém grandes quantidades de sulfeto de
hidrogênio. O sulfeto de hidrogênio contido no gás natural reage
primeiramente com metanol originando metilmercaptana, que então é convertida
em DMDS.
A
maior desvantagem na fabricação e no transporte da metilmercaptana para fins
industriais é o seu baixo ponto de ebulição, de apenas 6°C. Por sorte ela
pode ser facilmente transformada em uma substância química similar, o
dissulfeto de dimetila (DMDS), um líquido amarelo que ferve a 110°C. Este
composto consiste em duas moléculas de metilmercaptana unidas entre si pelos
átomos de enxofre. O DMDS é ligeiramente menos odorífico que a
metilmercaptana, mas é muito mais fácil e seguro de transportar, sendo a
maior parte deste produto produzido na cidade de Lacq, situada no sudoeste
da França, onde o gás natural contém grandes quantidades de sulfeto de
hidrogênio. O sulfeto de hidrogênio contido no gás natural reage
primeiramente com metanol originando metilmercaptana, que então é convertida
em DMDS.
A metilmercaptana é usada
industrialmente para fabricar pesticidas, especialmente para eliminar ervas
daninhas das colheitas como trigo, milho e arroz. A sua principal utilização
na indústria é para regenerar o catalisador usado no refino do petróleo.
Metilmercaptana também é usada para fazer a metionina, um aminoácido que
pode ser deficiente em nossa dieta.
Algumas rações para animais
são hoje fortificadas pela adição de metionina, aumentando conseqüentemente
a sua quantidade na carne e no leite.
Home | Anidridos | Ácidos Sulfônicos | Haletos de Ácido | Organometálicos | Tiocompostos
Este site foi atualizado em
12/07/10