 CICLOS
BIOGEOQUÍMICOS
CICLOS
BIOGEOQUÍMICOS
ÍNDICE
2.3. OS COMPONENTES DO ECOSSISTEMA
4. FATORES DE DESEQUILÍBRIO AMBIENTAL
4.2. CONCENTRAÇÃO DE POLUENTES NOS NÍVEIS TRÓFICOS
5.1. EFEITOS TÓXICOS CAUSADOS PELO MERCÚRIO
5.2. USO DO MERCÚRIO NO BRASIL
5.2.2. MERCÚRIO COMO CONTAMINANTE AMBIENTAL
5.2.3. A CONTAMINAÇÃO POR GARIMPOS DE OURO
5.2.4. O ACIDENTE DA BAÍA DE MINAMATA
5.2.5. AS DIFERENÇAS ENTRE A AMAZÔNIA E MINAMATA
5.3. EFEITOS TÓXICOS CAUSADOS PELO CHUMBO
O termo ecologia foi utilizado pela primeira vez em meados de 1870 pelo biólogo alemão Ernst Haeckel, discípulo de Charles Darwin, para designar a ciência das relações dos organismos com o meio ambiente.
A palavra ecologia deriva de duas palavras de origem grega: olkos, que significa casa, ou em um sentido mais amplo, ambiente, e logos, que quer dizer ciência ou estudo. Dessa forma, ecologia significa ciência do ambiente, ou, em uma definição mais completa, pode ser entendida como a ciência que estuda as relações entre os seres vivos e o ambiente onde vivem. Atualmente, a designação que tem sido mais utilizada, define a ecologia como sendo a ciência que estuda os ecossistemas.
Os níveis de organização e os âmbitos da ecologia
Nos dias atuais, a ecologia passou a ser um dos temas de maior destaque nos meios de divulgação. Isso se deve em grande parte aos desastres ecológicos que se sucedem não apenas em nosso país mas também em vários outros, de tal maneira, que a ecologia passou a adquirir grande importância prática.
O Homem é o ser vivo que mais agride o ambiente em que vive, sendo que até certo tempo atrás ele acreditava que poderia interferir no meio ambiente da maneira que lhe fosse mais conveniente. Aos poucos, porém, ele foi percebendo que o descarte inadequado dos subprodutos de suas indústrias, o uso indiscriminado de agrotóxicos, e o descuido com rios, lagos e fontes não só acabava com a vida existente nesses meios, mas também trazia enormes transtornos a ele próprio, pois uma vez que o Homem alterava o meio onde vivia, a natureza lhe respondia cada vez mais de uma maneira mais ríspida e rápida.
Hoje em dia se faz necessário conhecer as noções básicas da ecologia, ou seja, aprender como os seres interagem com o ambiente e verificar o papel deles no equilíbrio ecológico.
Sem sombra de dúvida,
o Homem já fez progressos consideráveis na tentativa de recuperar os
ecossistemas que foram destruídos e de preservar aqueles que poderiam ser
atacados. Um exemplo disso foi o encontro da comunidade científica
internacional em conjunto com políticos em junho de 1992, na cidade do Rio
de Janeiro, na conferência que ficou conhecida como ECO-92, durante a qual
foram discutidas soluções e responsabilidades de problemas que são comuns
aos países. O ponto alto desse encontro foi a elaboração da Carta da Terra.
Em contrapartida, a saída dos Estados Unidos, um dos maiores poluidores do
meio ambiente, do Tratado de Kioto foi uma prova cabal que não são todos que
aprenderam com as respostas da natureza. A defesa americana é simplesmente
insustentável, pois alega que com a assinatura do Tratado, a indústria
americana teria que se adequar a uma nova política de controle de emissão de
gases poluentes, e isso levaria a indústria a ter gastos extras e a ter que
fazer cortes de pessoal, o que poderia gerar uma crise na indústria
americana e, conseqüentemente, levaria a uma crise na economia mundial.
No início da formação do planeta, existia uma grande camada de gases, constituída basicamente de metano, amônia, vapor de água e hidrogênio. Com o passar do tempo, o planeta foi se resfriando, o que permitiu um acúmulo maior de água, originando os primeiros mares, ou mares primitivos.
Paralelamente a isso, a Terra ía sendo bombardeada constantemente pelos raios solares que faziam com que transformações físicas e químicas nos componentes da atmosfera e da crosta terrestre fossem ocorrendo. A partir desse momento, a vida se originou e nunca mais deixou de existir no planeta.
Com o aparecimento dos seres vivos, uma nova entidade passou a fazer parte da constituição do planeta, ou seja, além da litosfera, hidrosfera e atmosfera, a Terra passou a contar com a biosfera. A biosfera compreende todos os lugares do planeta onde existe vida. As camadas que envolvem o planeta recebem a terminação “sfera” devido ao formato esférico da Terra. Assim sendo, pode-se montar uma tabela para ilustrar o nome e o significado de cada um.
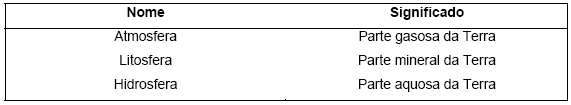
Uma afirmação que se pode fazer a respeito da biosfera é que a sobrevivência de todos os seres vivos que a compõem, com exceção de um pequeno grupo de seres procariontes quimiossintetizantes, depende, em uma última análise, dos organismos clorofilados. Estes, por meio da fotossíntese, produzem o alimento que é utilizado por todos os outros seres vivos. Como subproduto da fotossíntese, as plantas liberam oxigênio, que é fundamental para a respiração de todos os seres vivos, sejam eles animais ou vegetais. Esse tipo de dependência que existe entre animais e vegetais é apenas um dos muitos exemplos de interações que ocorrem na biosfera.
Como regra, populações de espécies diferentes devem viver em constante
interação, formando as comunidades bióticas, ou biocenose. A biocenose
depende do conjunto de fatores físicos e químicos do meio, freqüentemente
chamado de biótopo. Uma comunidade biótica em interação com o conjunto de
condições físicas e químicas, da região onde ela habita, constitui um
ecossistema. Assim, temos:
BIOCENOSE + BIÓTOPO = ECOSSISTEMA
2.3. OS COMPONENTES DO ECOSSISTEMA
Um conjunto de seres vivos e o meio onde eles vivem, com todas as interações que estes organismos mantêm entre si, formam um ecossistema. Qualquer ecossistema apresenta dois componentes básicos: o componente biótico, que é representado pelos seres vivos, e o componente abiótico, que é representado pelas condições químicas e físicas do meio.
Em qualquer ecossistema, os representantes do componente biótico podem ser divididos em outros dois grupos: os autótrofos e os heterótrofos. O termo autótrofo é usado para designar os seres fotossintetizantes que conseguem captar a energia luminosa e utilizá-la para suprir suas necessidades energéticas. Já o termo heterótrofo é usado para denominar os organismos que necessitam captar, do meio onde vivem, o alimento que lhes forneça energia e matéria-prima para a sua sobrevivência. Dessa forma, os seres autótrofos são ditos produtores dos ecossistemas, pois são eles que produzem toda a matéria orgânica e energia que será utilizada como alimento por outros seres vivos. É por meio deles que toda a energia necessária para a manutenção da comunidade biótica entra no ecossistema.
Estrutura básica do ecossistema
Os heterótrofos são os consumidores dos ecossistemas: eles apenas utilizam o alimento produzido pelos autótrofos para assim sobreviver. Um grupo muito particular de heterótrofos são os decompositores, pois estes se utilizam de matéria orgânica morta como fonte de alimentação. Os decompositores são de grande importância, pois é a partir deles que muitos nutrientes são devolvidos ao meio ambiente, tornando assim cíclica a permanência desses nutrientes, conforme será visto mais adiante.
Em termos de fatores abióticos, estes podem ser classificados em físicos e químicos, sendo que temperatura, luminosidade e umidade são exemplos de fatores físicos. Entre os fatores químicos, pode ser citada a presença de água e de minerais no solo.
Ambiente terrestre (esquerda) e ambiente aquático (direita).
Dentre os fatores físicos, a radiação solar é a que ocupa lugar de destaque, pois ela é quem comanda a maioria dos outros fatores. Dela provém toda a energia necessária para a sobrevivência dos seres vivos, além de ser ela a responsável pela manutenção da temperatura no planeta. Essa manutenção da temperatura é fator fundamental na distribuição dos seres vivos na superfície da Terra. Além disso, a radiação solar também afeta outros fatores climáticos como umidade relativa do ar, pluviosidade, etc.
Com relação aos fatores químicos, pode-se dizer que a presença ou ausência de um determinado elemento na água é decisiva para a manutenção da vida em um dado ambiente. Por exemplo, a presença de fósforo, encontrado na forma de fosfato em alguns tipos de rochas, é fundamental, pois o fósforo é constituinte importante da matéria viva. Outros elementos, como o cálcio, o boro, o carbono, o nitrogênio e o oxigênio, são essenciais para a manutenção da vida, tanto animal quanto a vegetal, sendo que esses elementos ficam presentes no meio ambiente em uma forma cíclica, ou seja, de alguma maneira eles são retirados do meio, cumprem o seu papel, seja formar uma proteína ou um ácido nucléico, como no caso do nitrogênio, seja a de um fosfolipídio no caso do fósforo, e, de alguma forma, eles devem retornar ao meio para novamente se tornarem parte do ciclo.
Pela figura anterior, fica evidente a forma como a energia solar é transferida e utilizada por todos os seres vivos. Inicialmente, a energia que é produzida pelo sol e que chega à Terra é suficiente para que as plantas consigam realizar a síntese de matéria orgânica por meio do processo de fotossíntese, ou seja, esse processo fornece toda a energia necessária para os processos vitais e para que as plantas possam crescer e se desenvolver. Nesse processo de crescimento e desenvolvimento, as plantas vão produzindo e armazenando energia, sais minerais e matéria orgânica, que vão ser posteriormente passados para os organismos superiores, via cadeia alimentar.
A matéria orgânica que foi sintetizada pelas plantas contém energia, que por sua vez vai servir de alimento para manutenção de processos vitais e de crescimento para os animais. Inicialmente, essa energia é passada aos herbívoros e, em seguida, é passada via cadeia alimentar a todos os outros organismos superiores, inclusive o Homem. Caso esse mecanismo de transporte seja interrompido em algum ponto, a decomposição da matéria orgânica por ação de bactérias e fungos, faz com que todos os nutrientes voltem ao solo e possam ser reabsorvidos novamente, dando continuidade ao ciclo.
O esquema apresentado ilustra o conceito de cadeia alimentar, e inerente a esse conceito está o conceito de nível trófico, que será discutido um pouco mais tarde, mas de antemão já é possível perceber que cada organismo ocupa um lugar pré-determinado na cadeia alimentar, e em virtude de sua colocação na cadeia dependerá a sua colocação em um nível trófico ou não.
A pirâmide de energia mostra uma conseqüência natural das leis da termodinâmica, ou seja, parte da energia é dissipada ao passar de um nível trófico para outro, e em cada nível a energia é transformada, nunca criada. Além disso, ela indica os níveis de aproveitamento ou produtividade biológica da cadeia alimentar.
Exemplos de pirâmides de energia
Uma das características mais marcantes dos ecossistemas é que os organismos que os compõem podem ser agrupados de acordo com seus hábitos alimentares. Nesse caso, cada grupo em particular constitui aquilo que costuma se denominar nível trófico. De acordo com essa definição, o nível trófico nada mais é que o lugar onde cada grupo de organismos ocupa em um determinado ecossistema. A seqüência dos níveis tróficos representa o caminho que tanto a energia como a matéria percorre em um ecossistema.
A fonte de energia que mantém qualquer ecossistema é o Sol. Assim, a energia luminosa proveniente do Sol é captada e metabolizada pelos produtores, que na sua maioria são seres fotossintetizantes, portanto autótrofos. Incluem-se nesse grupo os vegetais clorofilados e os organismos quimiossintetizantes (algumas bactérias). Posteriormente, os herbívoros, ao se alimentarem dos produtores, obtêm parte dessa energia e, assim sucessivamente, a energia vai passando de nível trófico até a sua chegada aos organismos que estão no topo da cadeia alimentar.
Do total de energia armazenada pelo autótrofo na matéria orgânica produzida pela fotossíntese, parte é consumida por ele mesmo na respiração, o que lhe mantém vivo. Portanto só é passado para o nível trófico seguinte aquilo que o produtor não consumiu, e desse, uma parte é eliminada pelos excrementos e uma parcela considerável da energia do alimento é consumida como forma de energia de movimento. As sobras são incorporadas aos tecidos permanecendo à disposição do nível trófico seguinte. Assim, a cada nível trófico, vai ocorrendo uma perda de energia, principalmente na forma de calor, forma essa que os seres vivos não tem condições de reaproveitar. Portanto, a energia flui de um nível trófico a outro se possibilidade de retrocesso, numa única direção; daí vem a denominação de que o fluxo de energia é unidirecional.
O esquema a seguir ilustra o que foi dito. Os raios solares, assim que chegam às plantas, que são os produtores da cadeia alimentar e por isso se encontram na parte debaixo da pirâmide, transformam essa energia em matéria orgânica, que, por sua vez, vão servir de alimento e fonte de energia para todos os consumidores que estão na parte superior da cadeia, transferindo, assim, a energia para esses consumidores. Uma vez que os animais do topo da cadeia não tem como reciclar essa energia, uma parte dela se perde na forma de calor para o ambiente.
Ao contrário do que acontece com o fluxo de energia, o fluxo de matéria não é unidirecional; ele segue o caminho inverso, ou seja, o caminho cíclico. Principiamos o raciocínio pelos produtores, que são os seres que transformam a energia radiante do sol em alimento, inicialmente para si, e depois para os demais organismos vivos que compõem os níveis tróficos superiores através da alimentação. Assim que qualquer um desse seres que compõem os níveis tróficos morre, a matéria orgânica é absorvida pelos microrganismos decompositores que trazem de volta ao solo os sais minerais e outros elementos, tornando-os disponíveis para serem reaproveitados novamente por outros organismos.
Os ciclos biogeoquímicos são processos naturais que por diversos meios reciclam vários elementos em diferentes formas químicas do meio ambiente para os organismos, e depois, fazem o processo contrário, ou seja, trazem esses elementos dos organismos para o meio ambiente. Dessa forma, a água, o carbono, o oxigênio, o nitrogênio, o fósforo, o cálcio, entre outros elementos, percorrem esses ciclos, unindo todos os componentes vivos e não-vivos da Terra.
Sendo a Terra um sistema dinâmico, e em constante evolução, o movimento e a estocagem de seus materiais afetam todos os processos físicos, químicos e biológicos. As substâncias são continuamente transformadas durante a composição e a decomposição da matéria orgânica, sem escapar da biosfera, sendo, portanto recicláveis.
Um ciclo biogeoquímico pode ser entendido como sendo o movimento ou o ciclo de um determinado elemento ou elementos químicos através da atmosfera, hidrosfera, litosfera e biosfera da Terra.
Os ciclos estão intimamente relacionados com processos geológicos, hidrológicos e biológicos. Como exemplo, pode-se lembrar que um modesto conhecimento sobre o ciclo geológico (aqui referido como um conjunto dos processos responsáveis pela formação e destruição dos materiais da Terra, subdividido em ciclo hidrológico e ciclo das rochas) é valioso para o conhecimento e compreensão de nosso ambiente, que está intimamente relacionado aos processos físicos, químicos e biológicos.
Os caminhos percorridos ciclicamente entre o meio abiótico e o biótico pela água e por elementos químicos conhecidos, como C, S, O, P, Ca e N, constituem os chamados ciclos biogeoquímicos.
O estudo desses ciclos se torna cada vez mais importante, como, por exemplo, para avaliar o impacto ambiental que um material potencialmente perigoso, possa vir a causar no meio ambiente e nos seres vivos que dependem direta ou indiretamente desse meio para garantir a sua sobrevivência.
Portanto podemos denominar de ciclos biogeoquímicos ao movimento contínuo dos elementos químicos, do meio físico para os seres vivos e destes novamente para o meio físico. Assim sendo, os átomos dos elementos químicos presentes na natureza e nos seres vivos não são criados nem destruídos, mas constantemente reciclados.

Como já fora visto anteriormente, a matéria pode ser constantemente reaproveitada na natureza, ou seja, quando uma planta ou um animal morre, as bactérias e fungos que estão presentes nos solos dão início ao processo de decomposição desses seres, e nesse processo de decomposição são trazidos de volta ao solo sais minerais, água e outros elementos, como Na, K, P, N.
Uma vez que esses elementos estão disponíveis novamente no solo, ar ou no ambiente de maneira geral, o processo todo se reinicia, como se fosse uma grande engrenagem, ou seja, o nitrogênio que está no ar atmosférico é utilizado por algumas bactérias que se encontram nas raízes de algumas plantas, o fósforo é novamente incorporado pelos seres vivos para compor os fosfolipídios e assim sucessivamente.
Os ciclos biogeoquímicos estão intimamente relacionados com os processos geológicos, de tal forma que é praticamente impossível tentar entender um ciclo biogeoquímico sem antes saber o que se passou com o planeta, as transformações que ele sofreu e que ainda hoje continua a sofrer, visto que a Terra é um sistema que prima pelo equilíbrio dinâmico que possui.
A existência da comunidade de um ecossistema está ligada à energia necessária à sobrevivência dos seres vivos a ela pertencentes. De maneira geral, num ecossistema, existem vegetais capazes de realizar fotossíntese. Deles dependem todos os demais seres vivos. O Sol é a fonte de energia utilizada pelos vegetais fotossintetizantes, que transformam a energia solar em energia química contida nos alimentos orgânicos. Durante a realização das reações metabólicas dos seres vivos, parte da energia química se transforma em calor, que é liberado para o ecossistema. Assim a energia segue um fluxo unidirecional.

A energia flui unidirecionalmente ao longo do ecossistema e é sempre renovada pela luz solar. A matéria orgânica, porém, precisa ser reciclada e nesse processo participam os seres vivos. Em qualquer ciclo existe a retirada do elemento ou substância de sua fonte, utilização por seres vivos e devolução para a sua fonte. Como os recursos na Terra são finitos e a vida depende do equilíbrio natural desse ciclo, esse processo de reciclagem da matéria é de suma importância.
São elementos essenciais à vida,
disponível para os produtores, em forma molecular ou iônica.
Participam da trajetória, desde o meio inanimado, passando pelos organismos
vivos e retornando ao meio original.
Aproximadamente 40 elementos são incorporados aos organismos na forma de
compostos orgânicos complexos ou participam de uma série de reações químicas
essenciais às atividades dos seres vivos.
GRUPOS DE NUTRIENTES
Macronutrientes
- Participam em quantidades superiores a 0,2% do peso orgânico seco (p.o.s.)
:
O carbono (C), o hidrogênio (H), o oxigênio (O), o nitrogênio (N) e o
fósforo (P), participam em quantidades superiores a 1 % do p.o.s. dos seres
vivos, além do enxofre (S), do cloro (Cl), do potássio (K), do sódio (Na),
do cálcio (Ca), do magnésio (Mg) e do ferro (Fe).
Micronutrientes
- Participam em quantidades
inferiores a 0,2% do p.o.s. do ser vivo :
O alumínio (Al), o boro (B), o cromo (Cr), o zinco (Zn), o molibdênio (Mo),
o vanádio (V) e o cobalto (Co).
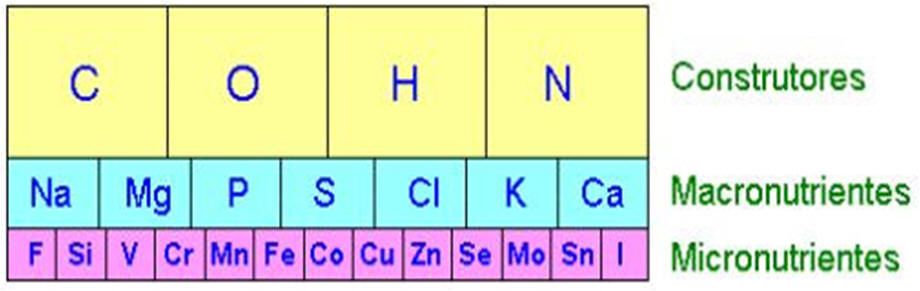
Os elementos essenciais que fazem parte desses ciclos recebem o nome de biogeoquímicos.
Portanto temos:
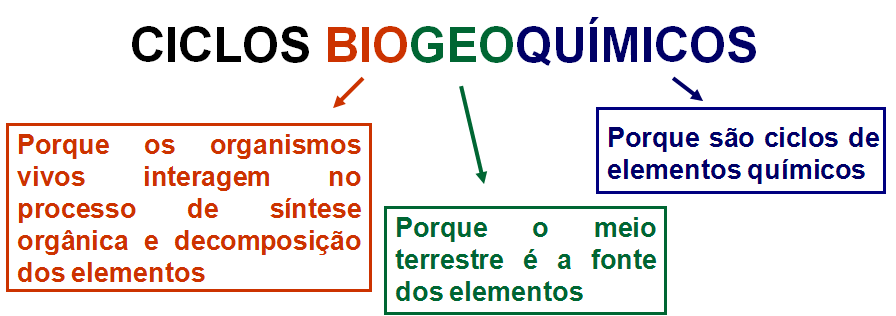
4. FATORES DE DESEQUILÍBRIO AMBIENTAL
O equilíbrio encontrado na natureza foi alcançado através de um lento e gradual processo de ajuste entre os seres vivos e o ambiente. O longo processo evolutivo que resultou na adaptação dos organismos ao ambiente é responsável pela harmonia das relações entre os seres vivos e o ambiente físico.
Os ciclos biogeoquímicos mostram como essa harmonia é facilmente identificada. Mesmo retirando grandes quantidades de elementos do ambiente, os seres vivos acabam, de uma forma ou de outra, devolvendo esses elementos ao meio, o que permite uma contínua renovação da vida.
A visão de uma natureza equilibrada capaz de resistir a tudo não mais faz parte do pensamento do homem moderno. É preciso que se tenha um bom senso, aliado a um pensamento crítico, de que a natureza aceita as mudanças impostas pelo homem até um certo ponto, e a partir desse ponto ela começa a sua reação, seja de uma forma ou de outra.
É provável que por causa da visão de que a natureza é uma fonte de recursos inesgotáveis e sempre capaz de se renovar, o homem tenha interferido de maneira tão abusiva, pondo em risco a sua própria estabilidade.
O lançamento de substâncias dos mais variados tipos no ambiente envolve dois tipos de problemas. Em um primeiro caso, ele pode ser tóxico ao próprio homem, chegando a ele pelos mais diversos meios, como ar, água ou pelos alimentos. Em um segundo caso, ele pode constituir ameaças indiretas ao homem, pois afetando o equilíbrio dos ecossistemas naturais, o homem põe em risco a sua vida, uma vez que ele depende diretamente desses ecossistemas para conseguir sobreviver.
Substâncias poluentes são aquelas que, quando lançadas no meio, representam um perigo em potencial à saúde dos organismos vivos. Dessa forma, é possível se classificar as substâncias poluentes em dois grandes grupos: poluentes quantitativos e qualitativos.
• Poluentes Quantitativos
São aqueles já existentes na natureza, mas também são liberados pelo homem
em quantidades significativamente maiores do que aquelas que ocorrem
naturalmente.
• Poluentes Qualitativos
São substâncias sintéticas, isto é, não ocorrem na natureza; a única forma
delas entrarem no ambiente é pela produção em fábricas e sua posterior
liberação para o ambiente.
Em termos dos perigos representados pelos poluentes quantitativos, sabe-se que quantidades adicionais de certas substâncias podem ser nocivas por causarem desequilíbrio nos ciclos biogeoquímicos, ou por sua concentração, acima dos níveis naturais, determinar toxidez para os seres vivos.
4.2. CONCENTRAÇÃO DE POLUENTES NOS NÍVEIS TRÓFICOS
Mesmo em pequenas quantidades no ambiente, os poluentes podem causar sérios desastres ecológicos ao ambiente, em grande parte devido à capacidade que esses poluentes têm de se concentrarem ao longo da cadeia alimentar e assim serem passados a níveis tróficos diferentes.
Enquanto grande parte da matéria e da energia que é transferida de um nível trófico para outro se perde, isso não acontece com certos tipos de poluentes. A esse processo de concentração dá-se o nome de magnificação trófica. Um dos exemplos mais marcantes é o DDT (diclorodifeniltricloroetano). O DDT é um pesticida organoclorado não biodegradável, largamente utilizado desde a década de 40. A ação efetiva do DDT fez com que as aplicações do produto fossem realizadas de uma forma cada vez mais generalizada e indiscriminada. Como conseqüência disso, muitas espécies inofensivas ou até úteis de insetos foram sumindo. O problema é que com o uso indiscriminado do DDT, com o passar do tempo, algumas classes de insetos começaram a desenvolver uma resistência a esse inseticida.
Iniciou-se, então, o uso de uma nova classe de inseticidas, os organofosforados, que embora sejam mais tóxicos que os primeiros e dotados de menor efeito residual, apresentam a vantagem de não criarem resistência.
Percebeu-se, com o passar do tempo, que o efeito residual, tido no começo como sendo muito vantajoso, era extremamente danoso ao ambiente e, conseqüentemente, ao Homem, pois os organoclorados não sendo biodegradáveis, tendem a se acumular no meio. A partir daí ocorre o fenômeno de magnificação trófica, mencionado antes, ou seja, as plantas incorporam esses organoclorados, que vão sendo passados, via alimentação para os mais diversos níveis tróficos.
O grande problema é que esses organoclorados têm a capacidade de se concentrarem no tecido adiposo dos animais, potencializando a sua ação, de tal forma que é muito comum encontrar animais com grandes concentrações de DDT.
Como pode ser visto no esquema acima, o destino final do DDT é o Homem, e de acordo com o fenômeno da magnificação trófica, é no Homem onde deverá ser encontrada a maior concentração de DDT, ou seja, o Homem usa o DDT para matar as pragas que atacam as culturas, mas sem se dar conta, ele acaba por provocar a sua morte também, de uma maneira lenta, gradual e dolorosa.
Um outro efeito do uso indiscriminado desses tipos de inseticidas é a destruição de um número muito grande de espécies consideradas úteis, ou seja, o pesticida não acaba somente com a praga, mas também com outras espécies. Um dos efeitos estudados em relação ao DDT é o fato de que algumas aves apresentaram uma queda acentuada em sua taxa de reprodução. Isso se deve à má formação das cascas das aves, o que as torna extremamente frágeis. Nesse caso, verificou-se que o DDT tinha uma ação decisiva e nociva no balanço hormonal das aves.
Entre os herbicidas mais utilizados atualmente, estão os compostos do ácido fenóxiacético (2,4D, 2,4,5T), as triazinas (atrazina, simazina), os compostos de uréia (diuron), os compostos de bipiridilo (diquat e paraquat), as piridinas cloradas (picloran). Todos esses herbicidas, além de potentes destruidores de vegetais, são extremante persistentes no solo.
Alguns herbicidas como a dioxina, também conhecida como agente laranja, possuem propriedades teratogênicas, ou seja, possuem ação deformante do feto em mulheres que se alimentem de vegetais contaminados. Esse efeito pode ser observado nas populações do Vietnã, onde durante o período em que ocorreu a guerra, o agente laranja foi usado indiscriminadamente e em larga escala pelos americanos, com o intuito de desfolhar as matas, para fins de observação e combate do avanço das tropas vietnamitas.
A contaminação por metais pesados é, sem dúvida alguma, umas das formas mais terríveis de poluição, pois os metais pesados apresentam, além de um grande efeito tóxico, um poder de acumulação nos seres humanos altíssimo, ou seja, além de contaminarem o ambiente de uma forma geral, contaminam o próprio Homem, causando efeitos danosos em grande extensão.
Dentre os metais pesados mais conhecidos, será dada uma ênfase maior ao mercúrio e ao chumbo.
5.1. EFEITOS TÓXICOS CAUSADOS PELO MERCÚRIO
A toxicidade dos sais inorgânicos de mercúrio é proporcional a sua solubilidade. O calomelano (Hg2Cl2) é um sal pouco solúvel que foi durante muito tempo utilizado como purgativo. Os íons de mercúrio têm a capacidade de formarem complexos muito fortes com os grupos –SH das proteínas (presentes no aminoácido cisteína) e sua toxicidade provavelmente se relaciona com a inativação das proteínas nas membranas celulares. Assim parece, pois os efeitos são particularmente notáveis nos rins e no cérebro, ambos nos quais a função das membranas celulares é muito importante, e também porque muitas bactérias e fungos morrem em contato com compostos de mercúrio. A atividade bactericida não específica tem sido freqüentemente relacionada com danos à membrana celular.
Os compostos inorgânicos de mercúrio, remédios, fungicidas, bactericidas etc, foram totalmente substituídos pelos chamados mercuriais orgânicos. É comum pensar nos metais como elementos formadores unicamente de sais (compostos iônicos), mas muitos deles podem formar compostos covalentes. O estanho e o chumbo são bons exemplos, e o mercúrio em particular tem a capacidade de formar ligações covalentes facilmente e em especial com compostos aromáticos. Um bom exemplo é o semesan, muito utilizado como fungicida e praguicida.
A vantagem de seu uso está na possibilidade de se controlar sua solubilidade pela inclusão nos substituintes apropriados ao mesmo tempo em que a ligação Hg-benzeno é tão estável que ela forma o íon R-Hg+, ainda capaz de reagir com grupos –SH e formar derivados do tipo R-Hg-SH-proteína.
Compostos insolúveis, como o semesan, têm sido amplamente utilizados para impregnar sementes e protegê-las no solo dos ataques de pragas. O problema é que numerosos acidentes têm ocorrido quando essas sementes foram usadas por pessoas desavisadas na preparação de alimentos.
Em 1969, houve um decréscimo acentuado da população de pássaros em torno dos lagos na Suécia central. Foram afetados especialmente os pássaros que se alimentavam de peixes. Seus tecidos continham níveis surpreendentemente altos de mercúrio, mas a natureza de sua dieta não indicava que se tivessem envenenado por sementes tratadas com compostos de mercúrio. Suspeitou-se, então, da poluição industrial causada pelas fábricas ao redor do lago, que produziam derivados da polpa da madeira. A princípio suspeitou-se de que os fungicidas com mercúrio, adicionados para a preservação da madeira, teriam sido concentrados ao longo da cadeia alimentar; depois, suspeitou-se do próprio mercúrio elementar liberado acidentalmente pela fábrica de soda cáustica. Assim, a história seria paralela à de Minamata (que será vista adiante).
5.2. USO DO MERCÚRIO NO BRASIL
O mercúrio foi usado pela primeira vez no Brasil em meados do ano de 1850, durante o início do ciclo de exploração do ouro. Durante o ciclo do ouro, estima-se que a emissão total de mercúrio no ambiente foi algo em torno de 500 toneladas, ou seja, cerca de 2 a 5 t/ano.
Com o acelerado processo industrial brasileiro em meados da década de 50, o mercúrio teve seu uso bastante difundido, chegando ao ápice na década de 70, com uma média de utilização em torno de 100 t/ano.
Com a demanda da atividade de garimpo a partir de 1984, o consumo de mercúrio praticamente dobrou, em particular nos estados de Mato Grosso, Pará e Rondônia, onde essa atividade era mais intensa devido à presença de imensas jazidas de ouro.
Os garimpeiros usam o mercúrio devido à sua alta capacidade de solubilizar outros metais a frio, inclusive o ouro, formando amálgamas. Misturado ao solo, ou a sedimentos de fundo de rio, o mercúrio consegue ligar-se a minúsculas partículas de ouro ali presentes, permitindo dessa maneira a sua separação. Em seguida, queimase o amálgama, volatilizando o mercúrio e recuperando-se todo o ouro que venha estar presente. Esse processo é bastante atraente devido à sua simplicidade e mais ainda pelo seu baixo custo.
5.2.2. MERCÚRIO COMO CONTAMINANTE AMBIENTAL
Entre os metais potencialmente danosos ao ambiente, o mercúrio destaca-se dos outros por suas características químicas ímpares. O mercúrio pode existir no ambiente sob inúmeras formas, o que torna sua distribuição ambiental bastante complexa.
Quando emitido na forma de vapor, o mercúrio tem um tempo de residência na atmosfera que pode variar de alguns dias até anos. Parte desse mercúrio deposita-se no local e parte se incorpora à circulação atmosférica. A oxidação do metal Hg0 → Hg2+, por diversos processos, o torna altamente solúvel, o que facilita a sua deposição pela ação da gravidade ou por intermédio das chuvas. Dessa forma, quando se fala no impacto causado pelo mercúrio, deve sempre ser levado em conta a sua forma química.
O mercúrio inorgânico liberado nas formas metálica ou gasosa pode originar compostos organometálicos como o dimetilmercúrio ((CH3)2Hg) e o íon metilmercúrio (CH3Hg+), sendo essas as mais danosas formas de contaminação.
A síntese do CH3Hg+ a partir do Hg2+ é mediada por diversos tipos de microrganismos presentes em organismos aquáticos.
Por muito tempo pensou-se que o sedimento do fundo de rios e lagos fosse o principal local da formação do CH3Hg+, mas essa reação já havia sido observada em outros tipos de substrato, como em algas que crescem em raízes de plantas aquáticas, outras superfícies submersas e também no próprio solo. Além disso, existem bactérias capazes de fazer a conversão do mercúrio orgânico a metilmercúrio. Embora o CH3Hg+ represente uma parcela muito pequena em sistemas aquáticos, ele é a forma dominante em organismos superiores, devido ao efeito da biomagnificação.
Em certas bacias hidrográficas, a produção e a disponibilidade de CH3Hg+ são maiores, mesmo não havendo fontes próximas de liberação de mercúrio, como os garimpos. Isso se dá em águas que apresentam uma natureza ácida, pois são ricos em matéria orgânica dissolvida e são pobres em nutrientes. Dessa forma, a água poderia funcionar como uma espécie de reator biogeoquímico, aumentando consideravelmente a concentração e a atividade tóxica do agente contaminante.
5.2.3. A CONTAMINAÇÃO POR GARIMPOS DE OURO
Os garimpos de ouro na Amazônia empregam diretamente entre 400 a 600 mil pessoas, sendo que nessa região são produzidos algo em torno de 100 toneladas de ouro anualmente.
O ouro encontrado nessa região ocorre como partículas finas, em terraços sedimentares e sedimentos ativos de rios. Os garimpeiros utilizam várias técnicas de pré-concentração gravimétrica e amalgamação com mercúrio. O amálgama é então queimado e, dessa forma, o mercúrio é liberado para a natureza.
Uma vez formado, o CH3Hg+, que é altamente solúvel e estável na água, apresenta um longo tempo de residência em organismos, com altos teores de bioacumulação na biota aquática.
O mapa da figura a seguir apresenta as localidades potencialmente afetadas pelo uso do mercúrio. Observa-se que a grande maioria das localidades afetadas se encontra em regiões onde a atividade garimpeira é mais intensa. Uma exceção é a região do vale do Paraíba, onde não se tem uma atividade garimpeira muito intensa.
A figura a seguir ilustra mais detalhadamente o efeito da atividade garimpeira e o uso do mercúrio no ambiente. Como foi apresentado anteriormente, devido à atividade de garimpo ser muito concentrada na região Norte do país, o mapa apresenta um destaque maior nessa área.
As principais cidades ribeirinhas ficam no caminho do mercúrio, ou seja,
todo o mercúrio liberado das atividades de garimpo tende a seguir para o Rio
Madeira ou para o Amazonas. Como o mercúrio sofre o processo de
biomagnificação, a população ribeirinha fica exposta a riscos de
contaminação por mercúrio, pois sua principal fonte de alimentação são os
pescados retirados desses rios, que podem estar contaminados pelo mercúrio
que foi jogado a muitos quilômetros de distância das populações. A partir da
década de 80, com o reconhecimento dos danos causados pelo mercúrio,
diversos trabalhos foram realizados visando fazer um levantamento da real
contaminação da região, sendo que em certos pontos observou-se índice três
vezes superior ao permitido por lei.
Logo a seguir são ilustradas as reações que ocorrem com o mercúrio quando o metal atinge um reservatório.
5.2.4. O ACIDENTE DA BAÍA DE MINAMATA
A saga de Minamata remonta ao início do ano de 1908, quando a Nippon Nitrogen Fertilizer instalou-se na cidade. A empresa produzia acetaldeído e derivados de ácido acético e logo começou a se destacar no cenário nacional. Em 1941, a empresa começou a produzir cloreto de vinila, tornando-se um dos alicerces do Japão na Segunda Guerra Mundial. A empresa utilizava sulfato de mercúrio como catalisador na produção do ácido acético e de seus derivados, além de cloreto de mercúrio para a catálise do cloreto de vinila.
Durante o processo químico de metilação do acetileno, parte do mercúrio também era metilado, liberando grandes quantidades do metal nos efluentes da fábrica. O detalhe é que todos os rejeitos da fábrica eram lançados diretamente na baía de Minamata.
Na época, pouco se sabia acerca da toxicidade do metal, bem como a sua capacidade de se acumular na cadeia alimentar, e foi exatamente essa falta de informação o que ocasionou as proporções gigantescas que o acidente tomou, pois uma vez que as pessoas não sabiam o mal que as acometia, nem a sua causa, procurar uma solução era complicado.
Abaixo está representado o esquema de operação que a indústria utilizava em sua planta industrial na cidade de Minamata.
Em 1956, foi notificado o primeiro de uma série de casos que configurar-se-ia como o maior desastre envolvendo população humana e contaminação por metais pesados. Meses depois, as autoridades sanitárias organizaram um comitê de estudos sobre a doença. Inicialmente, eles suspeitaram de alguma doença infecto- ontagiosa. Pesquisas preliminares apontaram uma grande mortandade de peixes na baía, além de distúrbios neurológicos em gatos, que eram semelhantes aos que foram encontrados nas pessoas de Minamata.
As pesquisas indicaram que não se tratava de uma doença infecto-contagiosa, mas sim de algo que estaria relacionado com peixes e frutos do mar contaminados. Os primeiros elementos apontados como possíveis agentes da doença foram o selênio, manganês e o tálio. Só no primeiro ano, foram computados 52 casos da doença com 17 mortes. Meses depois, a companhia afirmava que os níveis de metal na baía estavam dentro dos padrões e que, portanto, os testes realizados não podiam comprovar contaminação por metais pesados.
Em dezembro de 1960, a Associação de Vendedores de Produtos do Mar decidiu boicotar todo e qualquer tipo de produto marinho proveniente da região de Minamata.
Em 1977, começou o processo de dragagem dos sedimentos do fundo da baía. Aterrou-se a região e instalaram-se redes para que se pudesse impedir o acesso de peixes contaminados para o mar aberto e vice-versa.
Em 1987, começou a dragagem da segunda área. Removeram-se os rejeitos do fundo da baía que em análise posterior registraram mais de 25 ppm de mercúrio.
O projeto de despoluição só terminou em 1991, mas somente há pouco, as redes que separavam a parte limpa da contaminada foram retiradas.
5.2.5. AS DIFERENÇAS ENTRE A AMAZÔNIA E MINAMATA
O CH3Hg+, devido à sua rápida absorção e migração pelos tecidos dos organismos e também devido à sua forte ligação com proteínas que contêm enxofre, acumula-se muito facilmente nos organismos inferiores e depois é passado para os superiores na cadeia alimentar.
Um fator importante a respeito da toxicologia do CH3Hg+ é que sua difusão pelas barreiras biológicas é muito rápida, sendo que praticamente 95% da amostra ingerida é absorvida pela corrente sanguínea. Outro fator que merece destaque é o fato de sua grande seletividade pelo sistema nervoso central, atacando principalmente as áreas corticais do cérebro.
Outro agravante que ocorreu em Minamata, foi o fato de que mesmo depois do aparecimento da primeira vítima, transcorreram-se quase dez anos até a identificação do agente causador da doença. Já na Amazônia, as autoridades têm pleno conhecimento do potencial efeito tóxico do CH3Hg+.
A via preferencial de contaminação do CH3Hg+ é o consumo de peixes, o que torna o problema ainda mais terrível, pois os peixes são a base da dieta das populações ribeirinhas.
Há ainda outro terrível agravante. No caso da baía de Minamata, o efluente industrial já continha o mercúrio sob a forma metilada, enquanto que na Amazônia, o mercúrio é lançado no ambiente como mercúrio elementar, líquido ou na forma de vapor. A forma de vapor do mercúrio, após sofrer oxidação na atmosfera volta sob Hg2+. Essa forma é bastante reativa, podendo sofrer metilação principalmente em lagos de várzea, reservatórios hidrelétricos e rios de água negra.
5.3. EFEITOS TÓXICOS CAUSADOS PELO CHUMBO
A toxicidade do chumbo é conhecida há muito tempo. Antigamente, as principais fontes de envenenamento por chumbo eram tintas, muitas vezes ingeridas por crianças, além dos reservatórios e encanamentos de água potável feitos à base de chumbo ou pintados com tintas à base de chumbo.
O grau de dissolução do chumbo é função da dureza da água Entende-se como água dura aquela com concentração de CaCO3 acima de 50mg/L. Alta concentração de chumbo pode ser encontrado em água mole e ligeiramente ácida, principalmente se nela estiverem presentes agentes quelantes naturais (ácidos húmicos), derivados da turfa.
Embora o chumbo seja pouco absorvido nos intestinos, ele é um metal tóxico de efeito cumulativo, concentrando-se nos ossos.
Com o advento do motor a explosão e a intensificação do uso desse tipo de motor, pode-se verificar a partir de 1910 um aumento na concentração de chumbo nas neves polares.
O motor a gasolina é muito exigente em relação ao seu combustível; esse deve se vaporizar facilmente quando aspirado para dentro do cilindro, porém deve queimar devagar quando da ignição. Hidrocarbonetos que não sejam ramificados e tenham relativa volatilidade, tais com heptano, são combustíveis pobres, principalmente porque as reações iniciais com o oxigênio produzem radicais livres. Em contrapartida, os hidrocarbonetos ramificados, como o isooctano, queimam muito mais vagarosamente porque a formação múltipla de radicais livres pára nos pontos de ramificações.
A solução adotada foi diminuir a velocidade de combustão pelo uso de substâncias que interrompem a série de reações (os chamados agentes antidetonantes), sendo que uma das mais bem sucedidas tentativas como agentes antidetonantes foi a utilização do chumbo-tetraetila e chumbo-tetrametila.
O problema da gasolina foi resolvido, mas o preço disso ficou muito alto. Estima-se que aproximadamente 0,8 mL dos compostos citados eram adicionados a cada litro de gasolina, o que correspondia a aproximadamente 2 gramas de chumbo por litro de gasolina. A quantidade de chumbo utilizada foi estarrecedora: 300.000 toneladas por ano nos EUA e cerca de 50.000 toneladas por ano no Reino Unido. O Brasil foi o primeiro país a abolir o uso do chumbo na gasolina.
As chumbo-tetralquilas são compostos voláteis extremamente venenosos que afetam diretamente o sistema nervoso central, mas é o chumbo inorgânico dos produtos de combustão que causa a maior preocupação, pois partículas finas de chumbo metálico ou de haletos de chumbo são emitidas e chegam aos pulmões. O chumbo parece ser absorvido pela corrente sangüínea muito mais eficiente a partir dos pulmões.
A poluição causada por partículas transportadas pelo ar, é, portanto, um fenômeno tipicamente urbano, já que são nos grandes centros industriais que estão a maioria da frota de veículos automotivos e as grandes indústrias, que também podem, dependendo do tipo de matéria com que trabalha, ser responsável pela liberação de fuligem ou algum tipo de efluente não tratado que porventura possa vir a conter chumbo.
Recentemente, no interior de São Paulo, um caso ganhou destaque na mídia. Nesse caso, a empresa responsável tinha em seu pátio escória de chumbo, o que comprometeu enormemente a área ao redor. O caso registrado ocorreu em Bauru, onde a empresa Acumuladores Ájax Ltda., uma das maiores fábricas de baterias automotivas do país, foi multada por poluição ambiental. Laudos de diversos órgãos comprovaram a contaminação por chumbo no solo, vegetação, animais e também em crianças nas proximidades da empresa. A CETESB realizou várias campanhas de amostragem de chumbo nas chaminés, no solo, águas subterrâneas, na vegetação e ainda no solo no entorno da indústria. Na última inspeção, foram constatadas emissões de poeiras fugitivas nas operações de fusão em fornos e no refino de lingotes de chumbo, além de derrames de resíduos de chumbo pelo pátio da indústria, propiciando emissão de material particulado para o ambiente, atingindo inclusive áreas fora dos limites da fábrica.
Os efluentes resultantes de lavagem de pátios, da operação de desmonte de baterias e do processo industrial, não eram totalmente captados pelas canaletas que os conduziam à estação de tratamento. Também foi constatada deficiência na armazenagem de resíduos contaminados com chumbo, propiciando a contaminação do solo, tanto na área interna, como externa da fábrica. Pelas análises feitas nos laboratórios da CETESB, observou- e que as concentrações de chumbo na atmosfera foram extremamente elevadas, com média de 9,7 μg/m3, chegando a alcançar valores de até 37,7 μg/m3. O padrão de Pb adotado pela CETESB na atmosfera é de 1,5 μg/m3.
Com isso, animais e hortaliças em propriedades próximas à fábrica, também ficaram contaminadas por chumbo. De acordo com pesquisas e estudos médicos, a contaminação por chumbo causa sintomas como anorexia, vômitos, convulsão, dano cerebral permanente e lesão renal irreversível, caracterizando uma doença chamada saturnismo. A empresa teria de elaborar um plano de recuperação total das áreas contaminadas, internas e externas, abrangendo solo, águas superficiais e subterrâneas e vegetação.
As demais exigências dizem respeito à instalação de equipamentos de controle de efluentes líquidos e gasosos, limpeza de roupas, equipamentos e máquinas, cuidados com o armazenamento, sistemas de ventilação, reprocessamento ou destinação final adequada de todos os resíduos gerados, cuidados com as operações de carga e descarga dos produtos manipulados e, até mesmo, a obrigatoriedade de se implantar uma "cortina" de árvores no perímetro do terreno da fábrica, para diminuir o arraste de poluentes pela ação dos ventos.
Considera-se que a água está poluída quando ela deixa de ser adequada ao consumo humano, quando os animais aquáticos não podem viver nela, quando as impurezas nela contidas a tornam desagradável ou nociva seu uso como recreativo ou quando não pode ser mais utilizada em nenhuma atividade industrial, pois seus uso implicaria em sérios danos.
Os rios, os mares, os lagos e os lençóis subterrâneos de água são o destino final de todo poluente solúvel lançado no ar ou no solo. O esgoto doméstico é o poluente orgânico mais comum da água doce e das águas costeiras, quando em alta concentração. A matéria orgânica transportada pelos esgotos faz proliferar os microrganismos, entre os quais bactérias e protozoários, que utilizam o oxigênio existente na água para oxidar seu alimento, e em alguns casos o reduzem a zero. Os detergentes sintéticos, nem sempre biodegradáveis, impregnam a água de fosfatos, reduzem ao mínimo a taxa de oxigênio e são objeto de proibição em vários países, entre eles o Brasil.
Ao serem carregados pela água da chuva ou pela erosão do solo, os fertilizantes químicos usados na agricultura provocam a proliferação dosmicrorganismos e a conseqüente redução da taxa de oxigênio nos rios, lagos e oceanos. Os pesticidas empregados na agricultura são produtos sintéticos, que se incorporam à cadeia alimentar, inclusive à cadeia alimentar humana.
Os casos mais dramáticos de poluição marinha têm sido originados por derramamentos de petróleo, seja em acidentes com petroleiros ou em vazamentos de poços petrolíferos submarinos. Uma vez no mar, a mancha de óleo, às vezes de dezenas de quilômetros, espalha-se, levada por ventos e marés, e afasta ou mata a fauna e as aves aquáticas. O maior perigo do despejo de resíduos industriais no mar reside na incorporação de substâncias tóxicas aos peixes, moluscos e crustáceos que servem de alimento ao Homem. Exemplo desse tipo de intoxicação foi o ocorrido na cidade de Minamata. A poluição marinha tem sido objeto de preocupação dos governos, que tentam, no âmbito da Organização das Nações Unidas, estabelecer controles por meio de organismos jurídicos internacionais.
A poluição da água tem causado sérios problemas ecológicos no Brasil, em especial em rios como o Tietê, no estado de São Paulo, e o Paraíba do Sul, nos estados de São Paulo, Rio de Janeiro e Minas Gerais. A maior responsabilidade pela devastação da fauna e pela deterioração da água nessas vias fluviais cabe às indústrias químicas, com tratamento inadequado, instaladas em suas margens, e ao despejo de esgoto doméstico não tratado.
Os rios vão lentamente sofrendo um processo de degradação até o ponto em que esse quadro se torna praticamente irreversível, ou seja, o rio torna-se impraticável tanto para recreação, consumo ou mesmo como fonte produtora de alimentos. Quando isso acontece, costuma-se dizer que o rio está morto, pois não existe vida aquática e os poucos organismos que estão presentes no rio, são seres anaeróbios.
A Revolução industrial, ocorrida na Inglaterra em meados do século XVIII, se caracterizou pela passagem da manufatura à indústria mecânica. A introdução de máquinas fabris multiplicou o rendimento do trabalho e aumentou a produção global. A Inglaterra, berço da revolução, adiantou sua industrialização em 50 anos em relação ao continente europeu e saiu na frente na expansão colonial.
Assim, o mundo assistiu a uma mudança sem precedentes na história. O mundo seria mais mecanizado do que jamais fora, a era da produção mecanizada viria a substituir a manufatura.
Juntamente com a Revolução Industrial, o mundo conheceu através dos tempos a outra face do progresso, a poluição e a destruição do meio ambiente. Um dos grandes vilões é sem dúvida a destruição ocasionada pela chuva ácida. Como se não bastasse provocar um buraco na camada de ozônio da alta atmosfera e ameaçar o planeta de superaquecimento, a poluição, nas suas diversas modalidades, também envenena a chuva, algo tão essencial à vida como o próprio ar. Em conseqüência, 10 mil lagos na Suécia estão praticamente mortos. Na Noruega, outros 2 mil perderam seus peixes. E na Alemanha, mais de 35% das florestas estão doentes. O Taj Mahal, um dos mais belos monumentos hindus, está perdendo a sua cor branca. E na Península de Yucatán, ao sul do México, a chuva está rapidamente destruindo obras da civilização Maia, que floresceu ali pelo menos 1500 anos antes da chegada do homem branco.
Como sempre, em todos os lugares onde a chuva está servindo de meio de transporte para a poluição, os vilões da história são as indústrias e os veículos que despejam no ar, todos os dias, toneladas de dióxido de enxofre e óxidos de nitrogênio. Esses gases reagem com o vapor de água e outros compostos químicos da atmosfera para formar o perigoso ácido sulfúrico e o ácido nítrico. Apesar dos compostos serem perigosos, o problema da chuva ácida está associado à degradação do meio ambiente a longo prazo.
Além de poluir rios, lagos e acabar com a flora e a fauna aquática, a chuva ácida se infiltra no solo liberando certos metais potencialmente tóxicos, como alumínio, chumbo e cádmio. Esses podem se introduzir na cadeia alimentar pelas plantas e acabar prejudicando o homem.
O raciocínio a ser empregado é bastante simples: existe uma relação direta entre a acidez das chuvas e a morte de peixes e plantas. A acidez mata algas, plâncton e insetos. Sem esta vida microscópica, os lagos não têm como oferecer alimento aos habitantes desse nicho; em conseqüência, desaparecem os peixes. Por fim, os pássaros, que sem ter o que comer, também desaparecem.
A chuva ácida é uma causa direta do desequilíbrio que ocorre no ciclo do enxofre. Com o aumento da poluição, aumenta a concentração de enxofre no ambiente e, por conseqüência, o nível de acidez da chuva. Esse acréscimo no nível de acidez é responsável direto pela lenta e gradual destruição do meio ambiente de uma forma geral.
O ar é formado por uma mistura de vários elementos e compostos distintos e, embora historicamente a sua composição tenha sofrido um processo de evolução, pode-se considerar que, para fins práticos, a sua composição permanece invariável, pelo menos em relação aos seus componentes principais.
Os elementos e compostos representados na tabela a seguir, com exceção do gás carbônico, são considerados invariáveis no gás atmosférico.
A poluição do ar é hoje uma das grandes preocupações do homem. A emissão de gases poluentes chegou a tal ponto que compromete seriamente a qualidade de vida dos seres vivos. Essa poluição pode ser mais sentida em áreas de grande concentração industrial e/ou populacional.
Embora a poluição do ar sempre tenha existido, como nos casos das erupções vulcânicas ou da morte de homens asfixiados por fumaça dentro de cavernas, foi somente na era industrial que esse tipo de poluição se tornou um problema mais grave. Ela ocorre a partir da presença de substâncias estranhas na atmosfera, ou de uma alteração importante dos constituintes desta, sendo facilmente observável, pois provoca a formação de partículas sólidas de poeira e de fumaça.
Em 1967, o Conselho da Europa definiu a poluição do ar nos seguintes termos: “Existe poluição do ar quando a presença de uma substância estranha ou a variação importante na proporção de seus constituintes pode provocar efeitos prejudiciais ou criar doenças”. Essas substâncias estranhas são os chamados agentes poluentes, e podem ser classificados em quatro grupos principais:
• monóxido de carbono;
• material particulado;
• óxidos de enxofre;
• hidrocarbonetos.
As causas mais comuns de poluição do ar são as atividades industriais, combustões de todo tipo, emissão de resíduos de combustíveis por veículos automotivos e a emissão de rejeitos químicos, em sua maioria, tóxicos e extremamente danosos, por fábricas e laboratórios.
O principal poluente atmosférico produzido pelo homem (o dióxido de carbono é elemento constitutivo do ar) é o dióxido de enxofre, formado pela oxidação do enxofre no carvão e no petróleo, como ocorre nas fundições e nas refinarias. Lançado no ar, ele dá origem a perigosas dispersões de ácido sulfúrico. Às vezes, à poluição se acrescenta o mau odor, produzido por emanações de certas indústrias, como curtumes, fábricas de papel e celulose, entre outras. O dióxido de carbono, ou gás carbônico, importante regulador da atmosfera, pode causar modificações climáticas consideráveis se tiver alterada a sua concentração. É o que ocorre no chamado efeito estufa, em que a concentração excessiva desse gás pode provocar, entre outros danos, o degelo das calotas polares, o que resultaria na inundação das regiões costeiras de todos os continentes. O monóxido de carbono é emitido sobretudo pela queima de combustíveis fósseis. Outros poluentes atmosféricos são: hidrocarbonetos, aldeídos, óxido de nitrogênio, óxido de ferro, chumbo e derivados, silicatos, flúor e derivados, entre outros.
No final da década de 1970, descobriu-se uma nova e perigosa conseqüência da poluição: a redução da camada de ozônio que protege a superfície da Terra da incidência de raios ultravioleta. Embora não esteja definitivamente comprovado, atribuiu-se o fenômeno à emissão de gases industriais conhecidos pelo nome genérico de clorofluorcarbonos (CFC). Quando atingem a atmosfera e são bombardeados pela radiação ultravioleta, os CFC, muito usados em aparelhos de refrigeração e em sprays, liberam o cloro, elemento que ataca e destrói o ozônio. Além de prejudicar a visão e o aparelho respiratório, a concentração de poluentes na atmosfera provoca alergias e afeta o sangue e os tecidos ósseo, nervoso e muscular.
Os efeitos desses poluentes sobre a saúde humana podem ser danosos. O monóxido de carbono liberado pelos automóveis tem a capacidade de se ligar à hemoglobina do sangue. Isso leva a uma inutilização de parte da hemoglobina no transporte dos gases respiratórios, ocorrendo asfixia e como conseqüência a morte.
Um dos agravantes dos problemas causados pelos poluentes atmosféricos é a chamada inversão térmica. Em condições normais, a temperatura da atmosfera diminui proporcionalmente à medida que a altitude aumenta, havendo portanto um gradiente de temperatura desde o solo até as camadas superiores da atmosfera, o que facilita a dispersão dos poluentes.
Em certas situações, porém, o gradiente de temperatura é quebrado pela interposição de uma camada de ar quente entre as camadas frias localizadas a uma certa altitude, o que impede a dispersão de poluentes para o alto.
Um outro problema muito grave que também é
causado pela poluição da atmosfera é o chamado efeito estufa. Devido a seus
efeitos, ele será estudado com maior cuidado.
A atmosfera da Terra é constituída de gases que permitem a passagem da radiação solar e absorvem grande parte do calor (a radiação infravermelha térmica), emitido pela superfície aquecida da Terra. Essa propriedade é conhecida como efeito estufa. Graças a ela, a temperatura média da superfície do planeta mantém-se em cerca de 15°C. Sem o efeito estufa, a temperatura média da Terra seria de 18°C abaixo de zero, ou seja, ele é responsável por um aumento de 33°C. Portanto, é benéfico ao planeta, pois propicia totais condições para a existência e manutenção de vida.
Quando se alerta para riscos relacionados com o efeito estufa, o que está em foco é a sua possível intensificação, causada pela ação do homem, e a conseqüência dessa intensificação para o clima da Terra. A hipótese da intensificação do fenômeno é muito simples. Do ponto de vista da física, quanto maior for a concentração de gases, maior será o aprisionamento do calor, e, conseqüentemente, mais alta a temperatura média do globo terrestre. A maioria dos cientistas envolvidos em pesquisas climáticas está convencida de que a intensificação do fenômeno em decorrência das ações e atividades humanas provocará esse aquecimento. Uma minoria discorda disso e indaga em que medida esse aquecimento, caso esteja ocorrendo, se deve ao efeito estufa, intensificado pela ação do homem. Sem dúvida, as descargas de gases na atmosfera por parte das indústrias e das frotas de veículos contribuem para aumentar o problema e, naturalmente, ainda continuarão a ser objeto de muita discussão entre os cientistas e a sociedade.
A causa fundamental de todas as situações meteorológicas na Terra é o Sol e a sua posição em relação ao nosso planeta, não devendo entender-se por isto as variações estacionais que ocorrem ao mesmo tempo que a Terra progride na sua órbita anual. A energia calorífica fornecida pelo Sol afeta diretamente a densidade do ar (o ar quente é mais leve do que o ar frio), provocando assim todos os gradientes de pressão importantes que causam o movimento do ar numa tentativa de minimizar a distribuição deles. O movimento constante da atmosfera depende, assim, do balanço de energia, fator que temos de considerar sob dois aspectos: o balanço, ou "orçamento", entre a Terra e o espaço, porque este determina a temperatura média da atmosfera, e o balanço, ou "orçamento", no seio da atmosfera em si, porque este é a causa fundamental das condições meteorológicas.
O diagrama abaixo ilustra o processo de radiação na Terra.
O Sol emite radiação de onda curta a uma razão que varia pouco, pelo que é designada constante solar.
Essa emissão fornece a energia e calor para toda a vida natural e movimentos no nosso planeta. Quando atinge a Terra, a radiação solar é refletida, retrodifundida e absorvida por vários componentes: 6% é retrodifundida para o espaço pelo próprio ar, 20% é refletida pelas nuvens e 4% pela superfície do globo. Desse modo, 30% da radiação perde-se para o planeta por esses processos, que coletivamente constituem o albedo. As nuvens absorvem 3% da radiação solar restante, ao passo que o vapor de água, as poeiras e outros componentes no ar contam para mais 16%. O resultado de todas essas interferências atmosféricas é garantir que apenas 51% da radiação solar incidente atinja de forma efetiva e verdadeira a superfície do globo. Essa quantidade é apenas uma média na quantidade de radiação solar que chega ao solo em diferentes pontos do planeta. Pelo fato da Terra ser esférica, as regiões tropicais são atingidas por radiação solar três vezes mais do que as regiões polares. Além disso, devido à distribuição da nebulosidade, as regiões equatoriais recebem somente metade da radiação solar do que a recebida pelos desertos quentes e secos da Terra, onde cerca de 80% da radiação total que penetra na atmosfera atinge o solo. E nas latitudes médias nubladas, a radiação solar recebida no solo é somente um terço da que se encontra nos desertos.
A entrada da radiação solar tem de ser equilibrada de alguma forma. A forma encontrada é a saída de calor enviado pela Terra, o que resulta de radiação pela atmosfera. Ao contrário da radiação de onda curta, a radiação da Terra ocorre sob a forma de onda longa e é, por isso, muito mais absorvida pelo vapor de água e dióxido de carbono existentes na atmosfera. Da radiação emitida pelo globo terrestre (a parte sólida da Terra), cerca de 90% é absorvida pela atmosfera, que irradia cerca de 80% de novo para o solo. Deste modo, a atmosfera atua como uma cobertura ou como o vidro de uma estufa, e daí o chamado efeito estufa. Como resultado, apenas uma pequeníssima quantidade da radiação terrestre escapa diretamente para o espaço. O problema aparece justamente nesse ponto. O homem está cada vez mais adicionando dióxido de carbono na atmosfera. Ao queimar combustíveis fósseis para obtenção de energia também se tem adicionado gases de efeito estufa que não estão presentes naturalmente na atmosfera (óxido nitroso e o CFC). Juntando-se a isso o fato de que o homem cada vez mais continua a desmatar as florestas, tem-se uma equação simples, em que o aumento no desmatamento leva a um decréscimo na capacidade do ambiente por meio das árvores de se fazer a retirada do dióxido de carbono do ar, substituindo o CO2 por oxigênio.
Tudo isso faz com que, cada vez mais, menos radiação proveniente do Sol seja emitida de volta para o espaço. Quanto mais dióxido de carbono e outros gases de efeito estufa ficarem presentes no ar, mais radiação ficará sendo emitida de volta para a Terra. Quanto mais isto acontecer, mais a Terra ficará quente. E uma pequena mudança na temperatura global poderá acarretar uma série de problemas.
Uma das conseqüências imediatas que o aumento do efeito estufa causará é o aumento da temperatura global do planeta. Um dos efeitos causados pelo aquecimento global da Terra é a seca. Conforme aumenta a temperatura, mais água se aquecerá e evaporará. Se levarmos em conta lugares onde a chuva não tem uma precipitação pluviométrica regular, é fácil de se prever que os rios, que em muitos desses lugares não são perenes, tendem a desaparecer, comprometendo a vida vegetal, que é a base da cadeia alimentar.
Pode parecer um contra-senso, mas o inverso também já ocorre. Enquanto em algumas áreas há falta de água, outras irão ter água demais. Outro efeito do aquecimento global da Terra é o aumento no nível do mar. Se a temperatura da Terra continuar a aumentar nas regiões polares, grandes quantidades de gelo irão derreter, fazendo com que toda essa água vá direto para os oceanos. Toneladas e mais toneladas de gelo ficarão derretidas se a Terra aquecer-se o suficiente para isso, o que causará um aumento drástico no nível do mar.
Conforme pode ser visto, um aquecimento da temperatura da Terra acarreta grandes prejuízos para o meio ambiente e com conseqüências diretas para o homem, uma vez que o acréscimo da temperatura global leva a uma interferência direta no ciclo hidrológico, sendo que desse ciclo dependem muitas formas de vida.
O efeito estufa não é de forma alguma algo indesejável. Muito pelo contrário: como dito anteriormente, sem esse efeito não existiria vida na Terra. Ele é o responsável pelo aquecimento do planeta, mantendo-o a uma temperatura que propicia o nascimento e desenvolvimento das mais diversas formas de vida.
O que se faz prioritário é um cuidado maior do homem com as emissões sem prévio tratamento de poluentes ao meio ambiente.
Dentre as três formas de poluição, a que atinge o solo pode ser uma das mais danosas ao meio ambiente, pois é no solo onde se inicia grande parte dos ciclos biogeoquímicos.
O solo tem uma constituição dinâmica. Sua origem está ligada à desagregação de rochas e à decomposição de restos de animais e vegetais.
A sua porção mineral pode ser resultante da ação vulcânica ou da desintegração de rochas sólidas por ações físicas ou químicas reunidas sob a denominação genérica de intemperismo. Assim, grandes variações de temperatura ocorridas entre o dia e a noite, ou o congelamento de água em seus interstícios, constituem ações físicas do intemperismo. A presença de gás carbônico nas águas da chuva pode ser considerada como um fator de intemperismo químico.
A interação de todos esses fenômenos em conjunto leva a um desgaste natural e progressivo das rochas primárias da litosfera, que, juntamente com os produtos da decomposição orgânica, originam os solos férteis, próprios para a agricultura.
As três formas de poluição (na água, no ar e no solo) também interagem e, em conseqüência, têm surgido divisões inadequadas de responsabilidades, com resultados negativos para o controle da poluição. Os depósitos de lixo poluem a terra, mas sua incineração contribui para a poluição do ar. Carregados pela chuva, os poluentes que estão no solo ou em suspensão no ar vão poluir a água e substâncias sedimentadas na água acabam por poluir a terra.
A questão da contaminação do solo e das águas subterrâneas tem sido objeto de grande preocupação nas últimas décadas em países industrializados, principalmente nos EUA e nos países europeus. Esse problema ambiental torna-se mais grave para grandes centros urbanos, como por exemplo, a região metropolitana de São Paulo.
O encaminhamento de soluções para essas áreas contaminadas, por parte dos órgãos que possuem atribuição de administrar os problemas ambientais, deve contemplar um conjunto de medidas que assegurem tanto o conhecimento de suas características e dos impactos por ela causados, quanto da criação e aplicação de instrumentos necessários à tomada de decisão e às formas e níveis de intervenção mais adequados, sempre com o objetivo de minimizar os riscos à população e ao ambiente.
Uma das principais causas da poluição do solo é o acúmulo de lixo sólido, como embalagens de plástico, papel e metal, e de produtos químicos, como fertilizantes, inseticidas e herbicidas. O material sólido do lixo demora muito tempo para desaparecer no ambiente. O vidro, por exemplo, leva cerca de 5 mil anos para se decompor, certos tipos de plástico também demoram a se desintegrarem, pois são resistentes ao processo de biodegradação promovidos pelos microrganismos. As formas mais simples que podem ser usadas para reduzir o acúmulo de lixo, como a incineração e a deposição em aterros, também têm efeito poluidor, pois emitem fumaça tóxica, no primeiro caso, ou produzem fluidos tóxicos que se infiltram no solo e contaminam os lençóis de água. A melhor forma de reduzir o problema é investir maciçamente nos processos de reciclagem e também no uso de materiais biodegradáveis ou não descartáveis.
A poluição pode causar sérios danos ao solo, e dessa forma dificultar o cultivo. Nas grandes aglomerações urbanas, o principal foco de poluição do solo são os resíduos industriais e domésticos. O lixo das cidades brasileiras, por exemplo, contém de setenta a oitenta por cento de matéria orgânica em decomposição e constitui uma permanente ameaça de surtos epidêmicos. O esgoto tem sido usado em alguns países para mineralizar a matéria orgânica e irrigar o solo, mas esse processoapresenta o inconveniente de veicular microrganismos patogênicos. Excrementos humanos podem provocar a contaminação de poços e mananciais de superfície. Os resíduos radioativos, juntamente com nutrientes, são absorvidos pelas plantas. Os fertilizantes e pesticidas sintéticos são suscetíveis de incorporação à cadeia alimentar.
Fator principal da poluição do solo é o desmatamento, causa de desequilíbrios hidrogeológicos, pois em conseqüência de tal prática a terra deixa de reter as águas pluviais. Calcula-se que no Brasil sejam derrubados anualmente trinta mil quilômetros quadrados de florestas, com o objetivo de obter madeira ou áreas para cultivo.
Sem a proteção das matas, o solo fica exposto e, em conseqüência, nutrientes e sais minerais são perdidos pela ação das águas da chuva e do vento, e então o homem, para corrigir esse problema, cada vez mais adiciona fertilizantes ao solo, que como não consegue reter os nutrientes, vai se empobrecendo rapidamente. Vale recordar que um excesso de fertilizantes leva ao fenômeno da eutrofização de lagos.
• AMABIS, J. M e MARTHO, G. R. Curso básico de biologia. São Paulo, Moderna,
1993;
• AMABIS, J. M e MARTHO, G. R Biologia. São Paulo, Moderna, 1996;
• BRANCO, S.M Elementos de ciência do ambiente. São Paulo, Cetesb, 1980;
• CIÊNCIA HOJE No rastro do mercúrio, n° 153;
• DIAS, D. P. Biologia Viva. São Paulo, Moderna, 1996;
• ODUM, E. P. Ecologia. Trad. Christopher J. Tribe. Rio de Janeiro,
Guanabara,
1983;
• REMMERT, H. Ecologia. Trad. Maria Ferri Soares Veiga, São Paulo, Edusp/EPU,
1982;
• RODRIGUES, S. Zoologia. São Paulo, Cutrix, 1983;
• SCHLESINGER, W.H. Biogeochemistry: An analysis of global change. Academic
Press, 1991;
• TOMMASI, L. R. A degradação do meio ambiente. São Paulo, Nobel, 1977;
• WATT, K. E. F. Ecology and resources management. New York, Mc Graw-Hill,
1970;
• WESTHEIMER, F. H. Why nature phosphates. Science, 235;
• http://www.mec.gov.br/sef/ambiental/Guiaatividades-professor4.pdf;
• http://www.cve.saude.sp.gov.br/htm/chumbo_b.htm;
• http://www.fapesp.br/ciencia4718.htm;
• http://www.cetem.gov.br/html/mercurio/semiquanti/Prob.htm.